RCHD (המרכז הרפובליקני לפיתוח בריאות של משרד הבריאות של הרפובליקה של קזחסטן)
גרסה: פרוטוקולים קליניים של משרד הבריאות של הרפובליקה של קזחסטן - 2016
תסמונת גיליין-בארה (G61.0)
נוירולוגיה
מידע כללי
תיאור קצר
אושר
ועדה משותפת לאיכות השירותים הרפואיים
משרד הבריאות והפיתוח החברתי של הרפובליקה של קזחסטן
מיום 29 בנובמבר 2016
פרוטוקול מס' 16
תסמונת גילאן-בארה(תסמונת Guillain-Barré) (GBS) היא נגע אוטואימוני חריף המתקדם במהירות של מערכת העצבים ההיקפית, המתבטא בצורה של פרסטזיה של הגפיים, חולשת שרירים ו/או שיתוק רפוי (נוירופתיה חד-פאזית בתיווך חיסוני).
מילים נרדפות לתסמונת Guillain-Barré: פולינורופתיה דלקתית דה-מיאלינטיבית חריפה, פולינורופתיה אידיופטית חריפה, פולינויריטיס זיהומית (פולינוירופתיה), פולירדיקוליטיס חריפה, תסמונת Guillain-Barré-Strohlsyndrom, Landry-Guillain-Barrésyndrome, Landry-Guillain-Barrésyndrome-Syndrome-Landry-Guillainhl. -תסמונת Barré-Strohl), תסמונת לנדרי (תסמונת לנדרי), שיתוק עולה של לנדרי (Landery'sascendingparlysis), פוליו צרפתי (Frenchpolio) וכו'.
תכונה של מחלה זו היא מהלך מגביל עצמי, מונופאזי עם הישנות נדירות ביותר.
מתאם בין קודי ICD-10 ו-ICD-9
| CodeMKB-10 | קוד ICD-9 | ||
|
G61.0 |
תסמונת גילאן-בארה |
357.0 |
תסמונת גילאן-בארה |
תאריך פיתוח/עדכון הפרוטוקול: 2016
משתמשי פרוטוקול: רופאי משפחה, מטפלים, מחיימים, נוירופתולוגים (מבוגרים, ילדים).
סולם רמת הראיות:
| אבל | מטה-אנליזה איכותית, סקירה שיטתית של RCT או RCT גדולים עם סבירות נמוכה מאוד (++) להטיה שניתן להכליל את תוצאותיהם לאוכלוסייה מתאימה. |
| בְּ | סקירה שיטתית באיכות גבוהה (++) של מחקרי עוקבה או מקרה-ביקורת או מחקרי עוקבה או מקרה-ביקורת באיכות גבוהה (++) עם סיכון נמוך מאוד להטיה או RCT עם סיכון לא גבוה (+) להטיה, התוצאות מתוכם ניתן להרחיב לאוכלוסייה המתאימה. |
| מ |
מחקר עוקבה או בקרת מקרה או ניסוי מבוקר ללא אקראי עם סיכון נמוך להטיה (+). תוצאות שניתן להכליל לאוכלוסייה מתאימה או ל-RCT עם סיכון נמוך מאוד או נמוך להטיה (++ או +) שלא ניתן להכליל ישירות לאוכלוסייה מתאימה. |
| ד | תיאור של סדרת מקרים או מחקר לא מבוקר או חוות דעת מומחה. |
מִיוּן
מִיוּן
GBS מסווג הן כדלקת עצבית והן כמצב שלאחר זיהום. ישנן מספר צורות של GBS הנבדלות במהלך התהליך הפתולוגי, נקודת היישום העיקרית של תוקפנות אוטואימונית (מעטפת עצבית או מוט אקסונלי), פרוגנוזה של התאוששות וביטויים קליניים.
על פי תפיסות מודרניות, ישנם לפחות 8 זנים (גרסאות קליניות / תת-סוגים) של תסמונת Guillain-Barré:
1) פולינורופתיה דלקתית דלקתית חריפה (צורה קלאסית של תסמונת Guillain-Barré);
2) נוירופתיה אקסונלית מוטורית-חושית חריפה (AMSAN);
3) נוירופתיה מוטורית-אקסונלית חריפה (OMAN);
4) תסמונת מילר-פישר (MFS);
5) נוירופתיה פאנאוטונומית חריפה (תסמונת Guillain-Barré, Pandysautonomia חריפה);
6) גזע אנצפליטיס Bickerstaff (Bickerstaff);
7) וריאנט לוע-צוואר הרחם-ברכיאלי;
8) פולינוירופתיה גולגולתית חריפה.
ישנן גם אפשרויות לשילוב של תסמונת מילר-פישר עם צורות אחרות של תסמונת Guillain-Barré (תסמונת חפיפה MFS/GBS).
GBS מסווג גם לפי חומרת המצב בהתאם לביטויים הקליניים:
הצורה הקלה מאופיינת בהיעדר או פארזיס מינימלי, אשר אינו גורם לקשיים משמעותיים בהליכה ובטיפול עצמי;
עם חומרה בינונית, יש הפרה של הליכה, הגבלת תנועת החולה או צורך בעזרה או תמיכה מבחוץ;
בצורה חמורה של המחלה, החולה מרותק למיטה ודורש טיפול מתמיד, לעתים קרובות נצפתה דיספאגיה;
במצב חמור ביותר, החולים זקוקים לאוורור מלאכותי של הריאות (ALV) עקב חולשה של שרירי הנשימה.
קריטריונים נוירופיזיולוגיים לסיווג GBS(ר.
האדן,
ד.
קורנבלאת',
ר.
יוזטל., 1998).
קבוצה עם נגע דה-מיילינציה ראשוני:
נדרשת נוכחות של לפחות אחד מהסימנים הבאים בלפחות 2 עצבים או שני סימנים בעצב אחד אם כל שאר העצבים אינם מעוררים ומשרעת של תגובת M בנקודה הדיסטלית היא 10% או יותר מה גבול נורמלי תחתון:
מהירות התפשטות עירור (ERV) נמוכה מ-90% מהגבול התחתון של הנורמה, או פחות מ-85% כאשר משרעת תגובת ה-M בנקודה הדיסטלית נמוכה מ-50% מהגבול התחתון של הנורמה;
ההשהיה הדיסטלית של תגובת ה-M עולה על הגבול העליון של הנורמה ביותר מ-10%, או ביותר מ-20% אם משרעת תגובת ה-M בנקודה הדיסטלית היא מתחת לגבול התחתון של הנורמה;
נוכחות של פיזור או בלוק עירור;
זמן האחזור של גלי F חורג מהגבול העליון של נורמלי ביותר מ-20%.
קבוצה עם נגע אקסונלי ראשוני:
אין סימנים של דה-מיאלינציה המפורטים לעיל באף עצב (למעט כל סימן אחד בעצב 1, אם משרעת תגובת M בנקודה הדיסטלית היא יותר מ-10% מתחת לגבול התחתון של הנורמה), ולפחות ב שני עצבים המשרעת של תגובת M בנקודה הדיסטלית היא יותר מ-80% מתחת לגבול התחתון של הנורמה.
קבוצה עם עצבים לא מעוררים:
· לא ניתן לרשום את תגובת ה-M באף אחד מהעצבים הנחקרים או קיים רק בעצב אחד עם משרעת בנקודה הדיסטלית של יותר מ-10% מתחת לגבול הנורמלי התחתון.
קבוצה בלתי מוגדרת:
· שינויים שזוהו במהלך גירוי ENMG אינם עומדים בקריטריונים של אף אחת מהקבוצות לעיל.
אבחון (מרפאת חוץ)
אבחון ברמת אשפוז
קריטריונים לאבחון:
תלונות:
על חולשת שרירים גוברת בזרועות ו/או ברגליים;
חוסר תחושה וירידה ברגישות;
רגישות מוגברת (מישוש, טמפרטורה וכו') בידיים וברגליים;
כאבים בגב, בכתפיים ובחגורת האגן;
קושי בבליעה, גם מזון מוצק וגם נוזלים;
הפרה של תפקודי נשימה, עד היעדר נשימה עצמאית, עקב היחלשות שרירי הנשימה, היחלשות הקול ושיעול;
הפרעה בקצב הלב, בחלקן היא יכולה להיות מהירה מאוד, באחרות היא יכולה להיות מואטת;
שיתוק שרירי הפנים
הזעה מוגברת
תנודות בלחץ הדם
התרחשות אפשרית של פליטה בלתי מבוקרת של שתן;
אובדן רפלקסים בגידים
הליכה לא יציבה ולא יציבה, פגיעה בקואורדינציה של תנועות;
שינויים בנפח הבטן, זה קורה בגלל שקשה לאדם לנשום בעזרת הסרעפת, והוא נאלץ להשתמש בחלל הבטן;
ירידה בחדות הראייה - לרוב יש התפצלות ופזילה.
התסמינים טבועים הן במבוגרים והן בילדים ובילודים.
אנמנזה: GBS מתפתח, ככלל, 1-3 שבועות לאחר מחלה זיהומית (SARS, שפעת, סינוסיטיס, ברונכיטיס, דלקת ריאות, דלקת שקדים, חצבת, פרוטיטיס, שלשול וכו').
תסמינים נוירולוגיים מופיעים לפתע; רוב החולים מופיעים עם כאבים וכאבים.
בעת נטילת אנמנזה, חשוב להבהיר את ההיבטים הבאים.
נוכחות של גורמים מזרזים. בכ-80% מהמקרים, התפתחות תסמונת Guillain-Barré קודמת למחלות או מצבים מסוימים תוך 1-3 שבועות.
זיהומים של מערכת העיכול, דרכי הנשימה העליונות, יכולים להתפתח לאחר זיהום במעיים הנגרם על ידי Campylobacterjejuni, לאחר זיהומים הנגרמים על ידי נגיפי הרפס (ציטומגלווירוס, וירוס אפשטיין-בר, וירוס אבעבועות רוח), המופילוס אינפלואנזה, מיקופלזמות, חצבת, חזרת. borreliosis, וכו ' בנוסף, עם זיהום HIV, התפתחות של תסמונת Guillain-Barré אפשרי.
חיסון (נגד כלבת, נגד טטנוס, נגד שפעת וכו');
התערבויות כירורגיות או פציעות של כל לוקליזציה;
נטילת תרופות מסוימות (תרופות טרומבוטיות, איזוטרטינואין וכו') או מגע עם חומרים רעילים;
לפעמים תסמונת Guillain-Barré מתפתחת על רקע מחלות אוטואימוניות (זאבת אדמנתית מערכתית) וגידולים (לימפוגרנולומטוזיס ולימפומות אחרות).
יש דפוס מסוים בעלייה בסימפטומים, שעל פיו מבחינים בין 3 שלבים של המחלה:
התקדמות (1-4 שבועות) - הופעה והתעצמות של הפרעות נוירולוגיות;
רמה (10-14 ימים) - ייצוב התמונה הקלינית;
התפתחות הפוכה (ממספר שבועות עד שנתיים) - שיקום תפקוד תקין של הגוף.
בדיקה גופניתכולל:
· מצב סומטי כללי: מצב כללי וחומרתו, טמפרטורת גוף, מדידת משקל המטופל, בדיקת העור, נשימה, דופק, לחץ דם, מצב איברים פנימיים (ריאות, לב, כבד, כליות וכו').
· מצב נוירולוגי:
בדיקה נוירולוגית מכוונת לזהות ולהעריך את חומרת התסמינים העיקריים של תסמונת גיליין-בארה - הפרעות תחושתיות, מוטוריות ואוטונומיות.
הערכת כוחם של שרירי הגפיים;
מחקר של רפלקסים - לתסמונת Guillain-Barré, ארפלקסיה אופיינית (כלומר, היעדר רוב הרפלקסים);
הערכת רגישות - נוכחות של אזורי עור עם תחושת נימול או עקצוץ;
הערכת תפקוד איברי האגן - ייתכן בריחת שתן לטווח קצר;
הערכת תפקוד המוח הקטן - נוכחות של חוסר יציבות בתנוחת רומברג (עומד עם ידיים פרושות לפניו ועיניים עצומות), תנועות לא מתואמות;
הערכה של תנועות גלגלי העין - עם תסמונת Guillain-Barré, תיתכן היעדר מוחלט של היכולת להזיז את העיניים;
ביצוע בדיקות וגטטיביות - להערכת הנזק לעצבים המעצבבים את הלב;
תגובת הלב לעלייה חדה ממצב נוטה, פעילות גופנית מוערכת;
הערכת תפקוד הבליעה.
הערכה של חומרת הליקוי המוטורי בילדים מעל גיל 3 נעשית באמצעות סולם צפון אמריקה:
שלב 0 תסמונת Guillain-Barré היא הנורמה;
שלב 1 - הפרעות תנועה מינימליות;
שלב II - היכולת ללכת 5 מ' ללא תמיכה או תמיכה;
שלב III - היכולת ללכת 5 מ' עם תמיכה או תמיכה;
שלב IV - חוסר יכולת ללכת 5 מ' עם תמיכה או תמיכה (משורשר למיטה או לכיסא גלגלים);
שלב V של תסמונת Guillain-Barre - הצורך באוורור מלאכותי של הריאות;
שלב VI - מוות.
בתרגול קליני, כדי להעריך את חומרת הפרעות התנועה, נעשה שימוש בסולם כוח שרירי הגפיים (A. Szobor, 1976).
0 נקודות - אין תנועות בשריר.
1 נקודה - תנועות מינימליות בשריר, אך המטופל אינו מחזיק את משקל הגפה.
2 נקודות - המטופל מחזיק במשקל האיבר, אך ההתנגדות לחוקר מזערית.
3 נקודות - המטופל מתנגד למאמצים לשנות את מיקום הגפה, אך הוא חסר משמעות.
4 נקודות - המטופל מתנגד היטב למאמצים לשנות את מיקום הגפה, אך יש ירידה מסוימת בכוח.
5 נקודות - כוח השרירים מתאים לגיל ולנורמה החוקתית של הנבדק.
גרסאות קליניות של AIDP
| אוֹפְּצִיָה | תסמינים קליניים עיקריים |
| עם מצג קליני טיפוסי | |
| פוליראדיקולונורופתיה דלקתית חריפה (גרסת GBS טיפוסית) (>85%) | חולשה בגפיים עם הפרעות חושיות קלות יחסית (ייתכן שהפרעות תנועה בודדות). |
| פולינורופתיה אקסונלית מוטורית חריפה (>5%) | חולשה בגפיים ללא שינוי בתחושה. ניתן לשמר רפלקסים עמוקים. שחזור מהיר של פונקציות. נמצא בעיקר בילדים. |
| פולינוירופתיה אקסונלית מוטורית-חושית חריפה (>1%) | חולשה והפרעות תחושתיות בגפיים. התפתחות מהירה של ליקוי מוטורי חמור עם התאוששות איטית ולא מלאה. נמצא בעיקר אצל מבוגרים. |
| עם תמונה קלינית לא טיפוסית | |
| תסמונת מילר-פישר (>3%) | שילוב של אטקסיה, בעיקר מהסוג המוח הקטן, עם ארפלקסיה, אופתלמופולגיה ולעיתים חולשה קלה בגפיים. הרגישות נשמרת בדרך כלל. |
מחקר מעבדה:
KLA - כדי להוציא מחלה דלקתית של האיברים הפנימיים, מלווה בתסמונת פולינורופתית;
בדיקת סוכר בדם (כדי לא לכלול פולינוירופתיה סוכרתית);
בדיקות דם ביוכימיות - קריאטין, אוריאה, AST, ALT, בילירובין (כדי לא לכלול פולינוירופתיה מטבולית);
· בדיקת דם להרכב גזים, לריכוז אלקטרוליטים - בדיקות דם ביוכימיות עוזרות לשלול פולינוירופתיות מטבוליות;
PCR בדם עבור נגיפי הפטיטיס - למניעת תסמונת פולינורופתית בהפטיטיס
בדיקת דם לזיהום ב-HIV - כדי לא לכלול פולינוירופתיה הקשורה לזיהום ב-HIV;
· בדיקת דם PCR לאיתור זיהומים ויראליים (ציטומגלווירוס, וירוס אפשטיין-בר, בורליהבורגדורפרי, קמפילובקטרג'יוני ועוד) - אם יש חשד לאטיולוגיה זיהומית של GBS.
מחקר אינסטרומנטלי:
צילום רנטגן של איברי החזה - כדי לא לכלול מחלת ריאות דלקתית או סיבוכים ריאתיים נלווים עם היחלשות של שרירי הנשימה;
א.ק.ג - לאיתור או אי הכללה של הפרעות קצב לב וגטטיביות במרפאת GBS;
אולטרסאונד של איברי הבטן - מחלות של האיברים הפנימיים (כבד, כליות וכו') עלולות להיות מלוות בפולינוירופתיה בדומה ל-GBS;
· MRI של המוח *-דרוש לאבחנה מבדלת עם פתולוגיה של מערכת העצבים המרכזית (תאונה חריפה של כלי דם מוחיים, דלקת מוח);
MRI של חוט השדרה* - כדי לא לכלול נגעים (מיאליטיס) ברמה של עיבוי צוואר הרחם של חוט השדרה (C4 - Th2);
Electroneuromyography ** (ENMG) - עשויה להיות תקינה במהלך השבוע הראשון של המחלה, עם נזק לשרירים, מתגלה סוג דנרבציה של עקומת ENMG, הולכת הדופק איטית, סימני פגיעה במיאלין או באקסונים. לרוב, נבדקים השרירים הדיסטליים של הגפיים העליונות והתחתונות (למשל, tibialis anterior, extensor digitorum common) ובמידת הצורך, שרירים פרוקסימליים (למשל, quadriceps femoris).
*NB!
התוויות נגד מוחלטות ל-MRI הן: גוף זר מתכתי במסלול; מפרצת תוך גולגולתית חתוכה בחומר פרומגנטי; מכשירים אלקטרוניים בגוף (קוצב לב); אנמיה המטופואטית (לעיתות ניגוד).
התוויות נגד יחסית ל-MRI הן:
קלסטרופוביה חמורה;
תותבות מתכת, קליפסים הממוקמים באיברים לא סרוקים;
מפרצת תוך גולגולתית חתוכה בחומר לא פרומגנטי.
** NB! ENMG היא שיטת האבחון האינסטרומנטלית היחידה המאפשרת אישור נגעים של מערכת העצבים ההיקפית ואבחון GBS, בהתאמה, וכן להבהיר את אופי השינויים הפתולוגיים (דמיאלינציה או אקסונליים) ושכיחותם.
הפרוטוקול וההיקף של מחקרי ENMG בחולים עם GBS תלויים בביטויים הקליניים של המחלה:
- עם paresis דיסטלי בעיקר, עצבים ארוכים על הידיים והרגליים נבדקים: לפחות 4 מוטוריים ו-4 תחושתיים (חלקים מוטוריים ותחושתיים של העצבים המדיאניים והאולנאריים; עצבים פרונאליים, טיביאליים, עצביים פרונאליים וסוראליים שטחיים בצד אחד). הפרמטרים העיקריים של ENMG מוערכים:
תגובות מוטוריות (חביון דיסטלי, משרעת, צורה ומשך), נוכחות של בלוקים של עירור ופיזור תגובות מוערכת; מנתחת את מהירות ההתפשטות של עירור לאורך הסיבים המוטוריים באזורים הדיסטליים והפרוקסימליים;
תגובות חושיות (משרעת) ומהירות עירור לאורך סיבים תחושתיים בחלקים הדיסטליים;
· תופעות ENMG מאוחרות (גלי F): השהייה, צורה ומשרעת של תגובות, ערך chronodispersion, אחוז נשירה מנותחים.
- בנוכחות paresis פרוקסימלי, חובה ללמוד בנוסף שני עצבים קצרים (בית השחי, שרירי העור, הירך וכו') עם הערכה של הפרמטרים של התגובה המוטורית (חביון, משרעת, צורה).
יש לזכור כי הסימנים הראשונים לתהליך הדנרבציה מופיעים לא לפני 2-3 שבועות לאחר הופעת המחלה, וסימני תהליך העצוב מחדש - לא לפני 4-6 שבועות.
קריטריונים לאבחון עבור GBS קלאסימאת Asbury A.K. ו-Cornblath D.R.
בהתבסס על נתונים קליניים ומעבדתיים:
נוכחות של חולשה מוטורית מתקדמת עם מעורבות בתהליך הפתולוגי של יותר מאיבר אחד;
ארפלקסיה או היפו-רפלקסיה חמורה;
ניתוח CSF - נוכחות ב-1 μl של נוזל מוחי של לא יותר מ-50 מונוציטים ו/או 2 גרנולוציטים 2+.
המערכת לאבחון GBS, שהקריטריונים עבורה מנוסחים על ידי המכון הלאומי לחקר הפרעות נוירולוגיות ותקשורת ושבץ (ארה"ב):
קריטריונים נדרשים:
חולשה מוטורית מתקדמת ביותר מאיבר אחד;
חומרת הפרזיס משתנה מחולשה מינימלית ברגליים ועד טטרפלגיה;
עיכוב רפלקסים בדרגות שונות.
קריטריונים עזר לאבחון התסמונת:
1. החולשה גוברת תוך 4 שבועות מתחילת המחלה;
2. סימטריה יחסית של הנגע;
3. מידה קלה של הפרעות תחושתיות;
4. מעורבות בתהליך הפתולוגי של עצבי הגולגולת;
5. התאוששות;
6. תסמינים של חוסר תפקוד אוטונומי;
7. היעדר רגיל של תקופת חום בתחילת המחלה;
8. עלייה ברמת החלבון בנוזל השדרה (CSF) שבוע לאחר הופעת תסמיני המחלה, בתנאי שמספר הלויקוציטים החד-גרעיניים בדרך כלל לא יעלה על 10 תאים ל-1 מ"מ3;
9. הפרה של תפקוד המוליך של העצבים במהלך המחלה בכ-80% מהמקרים;
10. היעדר גורמים מבוססים לנזק עצבי היקפי, כגון השפעת הקסקרבון, פורפיריה, דיפתריה, מחלות רעילות וזיהומיות אחרות המחקות GBS.
סימנים ששוללים לחלוטין את האבחנה של GBS:
אסימטריה של paresis;
הפרעות חושיות בלבד;
הפרעות מתמשכות באגן
הפרעות בולטות באגן;
דיפטריה לאחרונה;
נוכחות של סימפטומים פסיכופתולוגיים - הזיות, דלוזיות;
הרעלה מוכחת עם מלחים של מתכות כבדות ואחרות.
אלגוריתם אבחון:
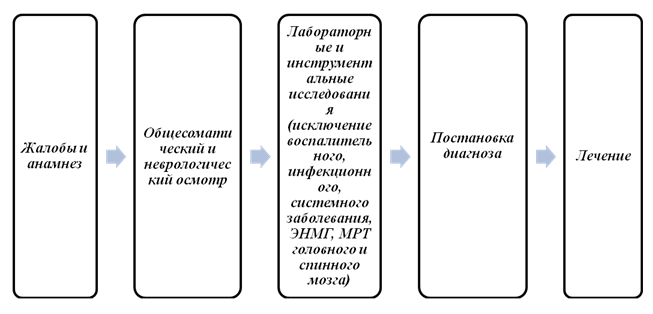
אבחון (בית חולים)
אבחון ברמה נייחת
קריטריונים לאבחון ברמת בית החולים:לראות רמה אמבולטורית.
תלונות ואנמנזה:לראות רמה אמבולטורית.
בדיקה גופנית:לראות רמה אמבולטורית.
* NB! הקריטריונים הניתנים בסעיף 9, סעיף קטן 1 אופייניים לצורות GBS, אקסונליות, פאראפארטיות ופרינגו-צווארי-ברכיאליות, וצורות כגון תסמונת מילר פישר ופנדיסאוטונומיה חריפה נבדלות באופן קליני באופן קליני מצורות אחרות של GBS, לכן, קריטריונים מקובלים לאבחון מחלה זו שקשה להם ליישם. האבחנה במקרים אלה נקבעת, קודם כל, על בסיס נתונים אנמנסטיים והתמונה הקלינית של המחלה.
מאפיינים של תסמונת מילר פישר.
מדהים, בלבול עקב היפונתרמיה הקשורה לייצור יתר של הורמון אנטי-דיורטי. עוויתות עלולות להתרחש כאשר תכולת הנתרן בפלזמה נמוכה מ-120 ממול/ליטר.
מאפיינים של פנדיסאוטונומיה חריפה.
התרחשות של תסמינים נוירולוגיים 1-2 שבועות לאחר זיהום ויראלי או חיידקי;
נוכחות של נגע מבודד של מערכת העצבים האוטונומית;
מערכת הלב וכלי הדם מושפעת לעתים קרובות (יתר לחץ דם תנוחתי, יתר לחץ דם עורקי, טכיקרדיה, הפרעות קצב לב);
ראייה מטושטשת, עיניים יבשות, הזעה;
תפקוד לקוי של מערכת העיכול (איליוס שיתוק);
קשיים במתן שתן, אצירת שתן חריפה;
הזעה מוגברת, צבע כחלחל של עור הידיים והרגליים, גפיים קרות;
מדהים, בלבול עקב היפונתרמיה הקשורה לייצור יתר של הורמון אנטי-דיורטי. עוויתות עלולות להתרחש כאשר תכולת הנתרן בפלזמה נמוכה מ-120 mmol/l;
ההחלמה היא הדרגתית ולעתים קרובות לא מלאה.
כדי לבצע אבחנה של תסמונת Guillain-Barré, יש צורך לקבוע בבירור את ההיסטוריה של התפתחות המחלה, יחד עם הערכת המצב הנוירולוגי, כדי להשוות אותה עם הקריטריונים לאבחון GBS (WHO; 1993). רצוי לבצע ניקור מותני עם מחקר של CSF, וכן לאשר את הרמה העצבית של הנגע ולברר את צורת המחלה על פי בדיקת ENMG.
אלגוריתם אבחון:
קודם כל יש להבדיל את GBS ממצבים שיכולים להוביל להתפתחות טטרפרזיס היקפית חריפה. חיפוש אבחון דיפרנציאלי מפושט מאוד כאשר משתמשים באלגוריתם ייחודי שפותח על ידי החוקרים של המוסד התקציבי של המדינה הפדרלית "NTsN" של האקדמיה הרוסית למדעי הרפואה.
אלגוריתם אבחון דיפרנציאלי עבור טטרפרזיס רפוי חריף (AFT)

הערה: OBT-acute flaccid tetraparesis; EMG אלקטרומיוגרפיה; פולינוירופתיה PNP; GBS - תסמונת Guillain-Barré; LP - ניקור מותני; BHAK - בדיקת דם ביוכימית; RF - גורם ראומטי; CRP - C-reactive protein; CPK - קריאטינין פוספוקינאז; MRI - הדמיית תהודה מגנטית (לא פחות מ-1 T); CT - טומוגרפיה ממוחשבת.
מחקר מעבדה:ראה רמת אשפוז (לאותן בדיקות שהיו רשומות בנוסף).
רשימת בדיקות מעבדה בסיסיות:
דם לאימונוגלובולינים - כאשר מתכננים טיפול ספציפי עם אימונוגלובולינים מסוג G, יש צורך לקבוע את שברי ה-Ig בדם, ריכוז נמוך של IgA בדרך כלל קשור למחסור התורשתי שלו, במקרים כאלה יש סיכון גבוה לפתח הלם אנפילקטי (טיפול באימונוגלובולינים הוא התווית נגד);
מחקר CSF (ציטוזה, ריכוז חלבון). בעת ניתוח נוזל מוחי, שלושת האינדיקטורים הבאים מיוחסים בדרך כלל למספר הקריטריונים האבחוניים המאשרים GBS:
נוכחות של תכולת חלבון גבוהה,
עלייה בשיעור האלבומין,
אין עלייה במקביל בציטוזיס.
בנוסף, ניתן להמליץ על בדיקות האבחון הבאות כדי לאשר את האבחנה ולהבהיר את התכונות של GBS במקרה מסוים:
· בדיקת דם לנוגדנים עצמיים לגנגליוסידים, עם מחקר חובה של GM1, GD1a ו-GQ1b אם למטופל יש הפרעות אוקולומוטוריות;
בדיקת דם לאיתור נוגדני IgA לקמפילובקטר ג'יוני;
· חקר התוכן של סמנים ביולוגיים של שרשראות כבדות של נוירופילמנטים, חלבון טאו וחלבון חומצי גליופיברילר בסרום הדם.
מחקר אינסטרומנטלי: ראה רמה אמבולטורית.
במקרים חמורים של המחלה (התקדמות מהירה, הפרעות בולבריות), ניטור יומיומי של לחץ הדם, א.ק.ג, דופק אוקסימטריה ובדיקת תפקוד הנשימה החיצונית (ספירומטריה, פיק זרימה), ניטור תפקוד הנשימה החיצונית (קביעת הנשימה החיצונית). קיבולת חיונית של הריאות (VC) צריכה להתבצע (בתנאים של היחידה לטיפול נמרץ). ) לזיהוי בזמן של אינדיקציות להעברת החולה לאוורור מכני.
אבחון דיפרנציאלי
יש להבדיל בין GBS ממחלות אחרות המתבטאות בפארזיס היקפי חריף, בעיקר מפוליו-מיאליטיס (במיוחד בילדים צעירים) ופולינוירופתיות אחרות (דיפתריה, עם פורפיריה). בנוסף, נגעים של חוט השדרה וגזע המוח (מיאליטיס רוחבי, שבץ במערכת הוורטברובזילרית) ומחלות עם פגיעה בהעברה עצבית-שרירית (myasthenia gravis, בוטוליזם) יכולים לקבל תמונה קלינית דומה.
|
אִבחוּן |
נימוק לאבחנה מבדלת |
סקרים |
קריטריוני אי הכללה אִבחוּן |
| פולומיאליטיס (במיוחד אצל ילדים צעירים) | פארזיס היקפי חריף |
· ENMG; מחט EMG; התייעצות עם מטפל; יִעוּץ אינפקציולוג. |
היסטוריה אפידמיולוגית; נוכחות של חום בתחילת המחלה; תסמינים של מערכת העיכול; אסימטריה של הנגע; היעדר הפרעות אובייקטיביות של רגישות; ציטוזה גבוהה בנוזל השדרה; האבחנה של פוליומיאליטיס מאושרת על ידי בדיקה וירולוגית או סרולוגית. |
|
פולינוירופתיות אחרות (דלקתיות: פולינוירופתיה דלקתית כרונית עם הופעה חריפה, מחלת סיוגרן, מחלת צ'ורג שטראוס, דלקת כלי דם קריוגלובולינמית; זיהומיות: קשור ל-HIV, מחלת ליים; רעיל: דיפטריה, פורפיריה, סמים, אלכוהול חריף, הרעלת מתכות כבדות דיסמטבולי: פולינוירופתיה של מצבים קריטיים, עם אי ספיקת כליות, כבד, פולינוירופתיה היפרגליקמית חריפה) |
פארזיס היקפי חריף |
· ENMG; מחט EMG; · מטפל נגד; · kons.nfektionista; בדיקות דם ושתן ביוכימיות |
סימנים לתהליך הדנרבציה-העצבה מחדש; פורפיריה נתמכת על ידי שילוב של פולינוירופתיה מוטורית בעיקרה עם כאבי בטן עזים, פארזיס במעיים, יתר לחץ דם עורקי, טכיקרדיה, שינויים נפשיים בולטים (מדכאון לדליריום), הפרעות שינה והתקפים אפילפטיים. לפריפורפיריה יש שינוי בצבע השתן, שהופך לאדמדם באור, ולאחר מכן לצבע חום-אדמדם עשיר. |
|
מיאליטיס רוחבי פגיעה ברמת עיבוי צוואר הרחם של חוט השדרה (C4 - Th2) פוסט זיהומי (M.pneumoniae, Schistosoma), לאחר חיסון, ויראלי (אנטרוווירוסים, הרפס), מיאליטיס הקשורה ל-HIV, עם מחלות דה-מיילינציה. של מערכת העצבים המרכזית, עם מחלות מערכתיות (זאבת אדומה מערכתית, מחלת סיוגרן, נמק חריף דלקת כלי דם) |
פארזיס היקפי חריף |
· MRI של חוט השדרה והמוח; · ENMG; חסרונות. מְרַפֵּא; cons.infectionist. |
גבול מגזרי של ליקוי חושי; הפרעות מתמשכות באגן חוסר מעורבות של שרירי חיקוי ונשימה בטטרפרזיס חמור. |
|
הפרה חריפה של מחזור עמוד השדרה, באגן vertebero-basilar. (פקקת של כלי חוט השדרה, מום כלי דם, מפרצת, דחיסה, טראומה, ניאופלזמה של חוט השדרה) |
פארזיס היקפי חריף |
· MRI של המוח וחוט השדרה; · ENMG; חסרונות. מְרַפֵּא; חסרונות. נוירוכירורג. |
התפתחות חריפה (בדרך כלל תוך מספר דקות); ברוב המקרים, דיכאון תודעה (תרדמת); אבחנה סופית מאושרת על ידי MRI של המוח/חוט השדרה. |
| מיאסטניה גרביס | פארזיס היקפי חריף | ENMG. |
השונות של הסימפטומים היעדר הפרעות תחושתיות; שינויים אופייניים ברפלקסים בגידים; האבחנה מאושרת על ידי EMG (גילוי תופעת ירידה); בדיקה תרופתית חיובית עם פרוזרין. |
| בּוּטוּלִיזְם | פארזיס היקפי חריף |
· ENMG; cons.infectionist. |
נתונים אפידמיולוגיים רלוונטיים סוג יורד של התפלגות של פארזיס, שימור מבחינת מקרים של רפלקסים בגידים, חוסר בהפרעות חושיות, אין שינוי בשאלה אם quore. |
טיפול בחו"ל
קבל טיפול בקוריאה, ישראל, גרמניה, ארה"ב
טיפול בחו"ל
קבל ייעוץ בנושא תיירות רפואית
יַחַס
תרופות (חומרים פעילים) המשמשים בטיפול
טיפול (אמבולטורי)
טיפול ברמת אשפוז
טקטיקות טיפול:
חשד לתסמונת Guillain-Barré, גם עם חומרת סימפטומים מינימלית, הוא הבסיס לאשפוז חירום, והטיפול הסימפטומטי מתבצע בשלב החוץ, ועם קביעת האבחנה הם נשלחים לבית החולים, והמטופל יש להזהיר את קרוביו מפני הידרדרות מהירה אפשרית של המצב.
לא סמיםיַחַס:לא.
טיפול רפואי:
טיפול סימפטומטי:
עם עלייה בלחץ הדם, ניתן לרשום nifedipine, 10-20 מ"ג מתחת ללשון;
כדי להפחית טכיקרדיה, נעשה שימוש ב-propranalol, במינון ראשוני של 20 מ"ג 3 פעמים ביום; אז המינון גדל בהדרגה ל-80-120 מ"ג ב-2-3 מנות, תחת שליטה של לחץ דם, קצב לב, אק"ג;
במקרה של ברדיקרדיה - אטרופין, למבוגרים: בולוס תוך ורידי בשליטה של אק"ג ולחץ דם - 0.5-1 מ"ג, במידת הצורך, ההקדמה חוזרת לאחר 3-5 דקות; המינון המרבי הוא 0.04 מ"ג/ק"ג (3 מ"ג). ילדים - 10 מק"ג / ק"ג;
כדי להפחית כאב, משככי כאבים, תרופות אנטי דלקתיות לא סטרואידיות ניתנות:
Ketorolac, דרך הפה פעם אחת במינון של 10 מ"ג או שוב ושוב, בהתאם לחומרת תסמונת הכאב, 10 מ"ג עד 4 פעמים ביום. המינון היומי המרבי לא יעלה על 40 מ"ג, או לא יותר מ-60 מ"ג ניתנים תוך שרירית עבור זריקה אחת; בדרך כלל 30 מ"ג כל 6 שעות.
דיקלופנק, תוך שרירית. מנה בודדת היא 75 מ"ג, המינון היומי המקסימלי הוא 150 מ"ג (עם הפסקה בין זריקה של לפחות 30 דקות).
איבופרופן, 1-2 טבליות 3-4 פעמים ביום; במידת הצורך - טבליה אחת כל 4 שעות. אין ליטול לעתים קרובות יותר מאשר לאחר 4 שעות. המינון היומי המרבי למבוגרים לא יעלה על 1200 מ"ג (לא יותר מ-6 טבליות ב-24 שעות).
אלגוריתם של פעולות במצבי חירום:אמצעי טיפול סימפטומטיים.
סוגי טיפול נוספים:לא.
התייעצות עם מומחה למחלות זיהומיות - הקמה או החרגה של מחלה זיהומית (מונונוקלאוזיס זיהומיות, מחלת ליים, HIV וכו');
התייעצות עם מטפל - הקמה או החרגה של מחלה טיפולית (מחלה דלקתית של איברים פנימיים: ריאות, כליות, כבד וכו');
התייעצות עם אנדוקרינולוג, נפרולוג, ראומטולוג - במידת הצורך, הדרה של פתולוגיה סומטית.
פעולות מניעה:
אין מניעה ספציפית של המחלה, רופאים עשויים להמליץ על טיפול בכל המחלות הזיהומיות ממש בתחילת התפתחותן, זה יפחית את ההשפעה השלילית של פתוגנים על מערכת העצבים.
ניטור מטופל:
הערכת מצבו הכללי של המטופל עם תיאור מצב העור; משקל החולה;
פרמטרים המודינמיים: מספר תנועות הנשימה, A/D, דופק, דופק;
הערכת מצב נוירולוגי.
טיפול אטיופתוגני אינו מתבצע בשלב זה, ולכן אין אינדיקטורים.
טיפול (אמבולנס)
אבחון וטיפול בשלב חירום
אמצעי אבחון:
לעתים קרובות, ל-GBS יש מהלך חריף והוא עלול לסכן חיים, מכיוון שהנגע מתקדם, מתפשט לעצבים הבולבריים ולעצבי גולגולת אחרים, החל מהרגליים, ולכן יש צורך באמצעים הבאים:
ציון בליעה- עם שיתוק בולברי, הפרעת בליעה, למניעת שאיבה
צינור האף.
הערכת נשימה- אולי התפתחות של אי ספיקת נשימה מתקדמת, ולא רק מהסוג חסימתי עקב שיתוק בולברי, אלא גם עם פגיעה בעצב הפרני (אופייני לסוג נשימה פרדוקסלי - בשאיפה דופן הבטן הקדמית שוקעת) ובין צלעית.
אינטובציה של קנה הנשימה (להמשך העברה של המטופל לאוורור מכני).
הערכת עבודת הלב:
· א.ק.ג -ירידה ואפילו היפוך של מקטע S-T, עלייה במרווח Q-T, דום לב אפשרי.
במהלך ההובלה חשוב להקפיד על שמירה על סבלנות דרכי הנשימה, מעקב קפדני אחר לחץ דם ודופק, טכיקרדיה, יתר לחץ דם אורתוסטטי, הפרעות קצב וכו'.
טיפול רפואי:
טיפול פוסינדורי לפי פרוטוקול למתן טיפול רפואי חירום.
טיפול (בית חולים)
טיפול ברמה נייחת
טקטיקות טיפול:מטרת הטיפול העיקרית היא: שיקום תפקודים חיוניים, העלמת סימפטומים של מחלה אוטואימונית באמצעות טכניקות ספציפיות, תקופת השיקום של המטופל ומניעת סיבוכים. הדבר הראשון שצריך לעשות הוא להכניס את החולה לבית חולים, ובמידת הצורך לחבר אותו למכונת הנשמה ריאות, להתקין צנתר אם יש הפרה של פליטת שתן, להתקין צינור אף אם הבליעה קשה.
טיפול לא תרופתי:
במקרים חמורים עם paresis חמור, טיפול נאות הוא בעל חשיבות מיוחדת כדי למנוע סיבוכים הקשורים לחוסר תנועה ממושך של החולה (זיהומים, פצעי שינה, תסחיף ריאתי). יש צורך לשנות מעת לעת (לפחות אחת לשעתיים) את עמדת המטופל, טיפול בעור, שליטה על תפקודי שלפוחית השתן והמעיים, התעמלות פסיבית, מניעת שאיפה. עם ברדיקרדיה מתמשכת, האיום של אסיסטולה עשוי לדרוש התקנה של קוצב לב זמני.
טיפול רפואי:
טיפול ספציפי לתסמונת Guillain-Barré, שמטרתו לעצור את התהליך האוטואימוני, משמש כיום בטיפול דופק עם אימונוגלובולינים מסוג G ופלזפרזה (ראה פסקה - סוגי טיפול אחרים). היעילות של כל אחת מהשיטות זהה יחסית, כך שהשימוש בו-זמני שלהן נחשב בלתי הולם.
אימונוגלובולינים מסוג G, כמו פלזמפרזיס, מפחית את משך השהייה באוורור מכני; זה ניתן לווריד מדי יום במשך 5 ימים במינון של 0.4 גרם/ק"ג. תופעות לוואי אפשריות: בחילות, כאבי ראש וכאבי שרירים, חום.
טיפול סימפטומטי בתסמונת Guillain-Barré מתבצע כדי לתקן הפרות של איזון חומצה-בסיס ומים-אלקטרוליטים, לתקן את רמות לחץ הדם ולמנוע פקקת ורידים עמוקים של תרומבואמבוליזם.
טיפול עירוי לתיקון הפרות של איזון חומצה-בסיס, מים-אלקטרוליטים, יתר לחץ דם עורקי חמור.
ליתר לחץ דם חמור מתמשך, נרשמות תרופות להורדת לחץ דם (חוסמי בטא או חוסמי תעלות סידן איטיות) (ראה יתר לחץ דם CP).
עם טכיקרדיה חמורה, חוסמי β (propranolol) נקבעים, עם ברדיקרדיה - אטרופין (ראה להלן).
עם התפתחות של זיהומים ביניים, יש צורך בטיפול אנטיביוטי (משתמשים בתרופות רחבות טווח).
למניעת פקקת ורידים עמוקים ותסחיף ריאתי, הפרין במשקל מולקולרי נמוך נקבע במינונים מניעתיים פעמיים ביום).
לכאבים ממקור נוציספטיבי (שרירי, מכני) מומלצים NSAIDs, במקרה של כאב נוירופטי, התרופות הנבחרות הן gabapentin, carbamazepine, pregabalin (רק למבוגרים!) (ראה להלן).
רשימת תרופות חיוניות:.
| הכנות | מנה בודדת | ריבוי מבוא |
| אימונוגלובולינים מסוג G | 0.4 גרם/ק"ג IV. | . 0.4 גרם/ק"ג ליום למשך 5 ימים פעם ביום, 5 ימים. |
| gabapentin | 300 מ"ג |
יום 1 300 מ"ג פעם אחת ביום, יום 2 300 מ"ג פעמיים ביום, יום 3 300 מ"ג 3 פעמים ביום, לאחר מכן, בהתאם לסבילות וליעילות האישיים, ניתן להגדיל את המינון ב-300 מ"ג ליום כל 2-3 ימים עד למקסימום של 3600 מ"ג ליום. |
| קרבמזפין | 200 מ"ג | מינון ההתחלה המומלץ הוא 200-400 מ"ג ליום. ניתן להעלות את המינון בהדרגה עד לקבלת אפקט קליני משביע רצון, במקרים מסוימים הוא יכול להיות 1600 מ"ג ליום. לאחר שתסמונת הכאב נכנסת להפוגה, ניתן להפחית את המינון בהדרגה. |
| פרגבאלין | 150 מ"ג | הטיפול מתחיל במינון של 150 מ"ג ליום, מחולק לשתיים או שלוש מנות. בהתאם לתגובה האישית של המטופל ולסבילות, לאחר 3-7 ימים ניתן להעלות את המינון ל-300 מ"ג ליום, ובמידת הצורך לאחר 7 ימים נוספים - עד למינון מקסימלי של 600 מ"ג ליום. |
רשימת תרופות נוספות:.
| הכנות | מנה בודדת | ריבוי מבוא |
| ניפדיפין | 10 מ"ג | 1-2 פעמים מתחת ללשון |
| פרופרנולול | 10 מ"ג | 20 מ"ג 3 פעמים ביום, לאחר מכן המינון גדל בהדרגה ל-80-120 מ"ג ב-2-3 מנות, בשליטה של לחץ דם, קצב לב, א.ק.ג. |
| אטרופין | 0,5-1,0 | מבוגרים: בולוס תוך ורידי בשליטה של א.ק.ג ולחץ דם - 0.5-1 מ"ג, במידת הצורך, ההקדמה חוזרת על עצמה לאחר 3-5 דקות; המינון המרבי הוא 0.04 מ"ג/ק"ג (3 מ"ג). ילדים - 10 מק"ג/ק"ג; |
| קטורולק | 10 מ"ג | דרך הפה פעם אחת במינון של 10 מ"ג או שוב ושוב, בהתאם לחומרת תסמונת הכאב, 10 מ"ג עד 4 פעמים ביום. המינון היומי המרבי לא יעלה על 40 מ"ג, או לא יותר מ-60 מ"ג ניתנים תוך שרירית עבור זריקה אחת; בדרך כלל 30 מ"ג כל 6 שעות. לא בשימוש בילדים. |
| דיקלופנק | 75 מ"ג | תוך שרירית, מנה בודדת של 75 מ"ג, המינון היומי המקסימלי הוא 150 מ"ג (עם הפסקה בין זריקה של לפחות 30 דקות). ילדים אינם מתאימים. |
| איבופרופן | 0.2 גרם |
1-2 טבליות 3-4 פעמים ביום; במידת הצורך - טבליה אחת כל 4 שעות. אין ליטול לעתים קרובות יותר מאשר לאחר 4 שעות. המינון היומי המרבי למבוגרים לא יעלה על 1200 מ"ג (לא יותר מ-6 טבליות ב-24 שעות). ילדים: 10-20 מ"ג/ק"ג 3 פעמים ביום למשך 2-3 ימים. |
התערבות כירורגית, מציינת אינדיקציות להתערבות כירורגית: ייתכן שיהיה צורך בהתערבות כירורגית עבור טרכאוסטומיה במקרה של אוורור מכאני ממושך (יותר מ-10 ימים), וכן גסטרוסטומיה במקרה של הפרעות בולבריות חמורות וממושכות.
סוגי טיפול נוספים:
יש לזכור תמיד את החשיבות יוצאת הדופן של מכלול אמצעי שיקום למניעת סיבוכים הנובעים מחוסר תנועה של המטופל ולשמירה על מצבם התפקודי של השרירים עד להופעת נפח מספק של תנועות עצמאיות.
המטופל צריך:
- פיזיותרפיה
- לעיסוי יש השפעה מיטיבה על חילוף החומרים, מה שמאיץ גם את צמיחת העצבים והעצוב מחדש
- פיזיותרפיה למניעת היווצרות התכווצויות (גירוי חשמלי, טיפול בחום, אלקטרופורזה תרופתית ועוד).
- טיפול בחמצן היפרברי.
פלזמה ממברנה מפחיתה באופן משמעותי את חומרת הפארזה ואת משך האוורור המכני. ככלל, 4-6 מפגשים מתבצעים במרווח של יום אחד; נפח הפלזמה שיש להחליף בפגישה אחת צריך להיות לפחות 40 מ"ל/ק"ג. כמדיה חלופית, נעשה שימוש בתמיסת נתרן כלורי 0.9% או reopoliglyukin.
יש לזכור על התוויות נגד לפלזמפרזיס (זיהומים, הפרעות בקרישת דם, אי ספיקת כבד), כמו גם סיבוכים אפשריים (הפרה של הרכב האלקטרוליטים, המוליזה, תגובות אלרגיות).
אינדיקציות לייעוץ מומחים:
התייעצות עם מומחה למחלות זיהומיות במידת הצורך (בהיעדר מומחה ברמה קדם-אשפוזית) - התקנת או הרחקה של זיהום כרוני (ברוצלוזיס, בורליוזיס וכו'), וכן במקרה של אישור של גורם זיהומי ל טיפול אטיולוגי נכון;
התייעצות עם מטפל במידת הצורך (בהיעדר מומחה ברמה טרום-אשפוזית) - הקמה או הרחקה של מחלה טיפולית (מחלה דלקתית של איברים פנימיים: ריאות, כליות, כבד וכו'), תיקון פרמטרים המודינמיים, אלקטרוליט. איזון במהלך הטיפול;
התייעצות עם רופא נמרץ - טיפול בחולים עם צורות חמורות של תסמונת Guillain-Barré מתבצע במשותף עם הרופא של היחידה לטיפול נמרץ;
התייעצות עם קרדיולוג - במקרה של הפרעות קרדיווסקולריות חמורות (יתר לחץ דם עורקי קשה מתמשך, הפרעות קצב).
אינדיקציות למעבר ליחידה לטיפול נמרץ והחייאה:
דרגה חמורה וחמורה ביותר של הפרעות נוירולוגיות;
חוסר יציבות המודינמית;
הפרה של תפקוד הנשימה.
מדדי יעילות הטיפול:
ייצוב המצב האימונולוגי (הרכב כמותי ואיכותי של דם IgG ונוזל מוחי);
רגרסיה של תסמינים נוירולוגיים מוקדים.
ניהול נוסף.
לאחר נורמליזציה של מצב בריאותו של המטופל, עליו להיות רשום אצל נוירולוג. בנוסף, יהיה צורך לעבור בדיקות מונעות על מנת לזהות את התנאים המוקדמים להישנות המחלה בשלב מוקדם. תצפית מרפאה במרפאה במקום המגורים.
לאחר תום התקופה החריפה, יש צורך בצעדי שיקום מורכבים, שתוכניתם נערכת על בסיס אינדיבידואלי, בהתאם לחומרת הסימפטומים השיוריים (טיפול בפעילות גופנית, עיסוי, בעוד הליכים תרמיים הם התווית נגד!).
חולים עם GBS. יש ליידע על הצורך לשמור על משטר ההגנה לפחות 6-12 חודשים לאחר סיום המחלה. עומס יתר פיזי, התחממות יתר, היפותרמיה, בידוד מופרז, צריכת אלכוהול אינם מקובלים. גם בתקופה זו יש להימנע מחיסונים.
שיקום רפואי
מתבצע בהתאם לתקן לארגון מתן שיקום רפואי לאוכלוסיית הרפובליקה של קזחסטן, שאושר בהוראת שר הבריאות של הרפובליקה של קזחסטן מיום 27 בדצמבר 2013 מס' 759.
טיפול פליאטיבי
בהתאם לסוג וחומרת הסיבוכים בעקבות המחלה, ייתכן שיידרש טיפול נוסף, כגון:
לחולים משובשים ניתן הפרין תת עורי במינון של 5,000 IU כל 12 שעות ודחיסה זמנית של שרירי השוק למניעת פקקת ורידים עמוקים;
לעיסוי יש השפעה מועילה על חילוף החומרים, אשר גם מאיץ את צמיחת העצבים ואת העצירות מחדש;
קינסיותרפיה הוכחה כמעוררת עצבנות מחדש ומשחזרת את נפח השרירים;
פיזיותרפיה לשיפור הכוח, למניעת היווצרות התכווצויות (גירוי חשמלי, טיפול בחום, אלקטרופורזה של תרופות);
· שיקום לפיתוח מיומנויות יומיומיות ושימוש במוצרים אדפטיביים המסייעים בחיי היום יום;
המטופל עשוי להזדקק לאורתוטיקה או למכשירי עזר אחרים כדי לשפר את התנועה.
פסיכותרפיה;
אִשְׁפּוּז
אינדיקציות לאשפוז מתוכנן:לא.
אינדיקציות לאשפוז חירום:
חולי GBS נתונים לאשפוז ביחידה לטיפול נמרץ.
מֵידָע
מקורות וספרות
- פרוטוקול ישיבות הוועדה המשותפת לאיכות השירותים הרפואיים של מחס"ד רקע, 2016
- 1. Bykova O. V., Boyko A. N., Maslova O. I. שימוש תוך ורידי באימונוגלובולינים בנוירולוגיה (סקירת ספרות ותצפיות משלו) // Nevrol. מגזין - 2000, 5. S.32-39. 2. Gekht B. M., Merkulova D. M. היבטים מעשיים של המרפאה והטיפול בפולינוירופתיה // Nevrol. כתב עת.-1997.-מס' 2.-C.4-9. 3. Piradov M.A., Suponeva N.A. תסמונת Guillain-Barré: אבחון וטיפול. מדריך לרופאים" -2011. 4. Suponeva N.A., Piradov M.A. "אימונותרפיה תוך ורידית בנוירולוגיה" -2013. 5. Sladky J. T. Guillain-Barre Syndrome בילדים // J. Child Neurol. 2004. ו' 19. עמ' 191–200. 6. Schmidt B., Toyka K. V., Kiefer R. et al. חדירות דלקתיות בביופסיות עצבים סורליות בתסמונת Guillain-Barre ונוירופתיה כרונית דלקתית demyelinating neuropathy // 1996. V. 19. P. 474-487. 7. Khalili-Shirazi A., Hughes R. A., Brostoff S. W. et al. תגובות תאי T לחלבוני מיאלין בתסמונת Guillain-Barre // J. Neurol. מדע 1992. V. 111. עמ' 200–203. 8. Van Rhijn I., Bleumink-Pluym N. M., Van Putten J. P. et al. DNA של קמפילובקטר קיים בתאים מיאלומונוציטים במחזור של אנשים בריאים ובאנשים עם תסמונת Guillain-Barre // J. Infect. Dis. 2002. V. 185. P. 262–265. 9. Cooper J. C., Ben-Smith A., Savage C. O. et al. שימוש חריג בגן פנוטיפ V של קולטן תאי T של תאי גמא דלתא T בשורה שמקורה בעצב היקפי של חולה עם תסמונת Guillain-Barre // J. Neurol. נוירוכירורגיה. פְּסִיכִיאָטרִיָה. 2000. ו' 69. עמ' 522–524. 10. Ilyas A. A., Chen Z. W., Cook S. D. ועוד. התפלגות תת-מחלקת אימונוגלובולין G של נוגדנים עצמיים לגנגליוסידים בחולים עם תסמונת Guillain-Barre // Res. קהילה. פאתול. פרמקול. 2002. ו' 109. עמ' 115–123. 11. Tsang R. S., Valdivieso-Garcia A. Pathogenesis of Guillain-Barre syndrome // Expert Rev. אנטי זיהום. ת'ר. 2003. V. 1. P. 597–608. 12. Kieseier B. C., Kiefer R., Gold R. et al. התקדמות בהבנה וטיפול בהפרעות בתיווך חיסוני של מערכת העצבים ההיקפית // עצב השריר. 2004. V. 30. P. 131–156. 13. Adams D., Gibson J. D., Thomas P. K. וחב'. אנטיגנים HLA בתסמונת Guillain-Barre // Lancet. 1977. מס' 2. עמ' 504–505. 14. Koga M., Yuki N., Kashiwase K. et al. תסמונות Guillain-Barre and Fisher שלאחר דלקת המעי של Campylobacter jejuni קשורות ל-HLA-54 ו-Cwl ללא תלות בנוגדנים אנטי-גנגליוסידים // J. Neuroimmunol. 1998. ו' 88. עמ' 62–66. 15. Magira E. E., Papaijakim M., Nachamkin I. ועוד. התפלגות דיפרנציאלית של אפיטופים HLA-DQ בטא/DR בטא בשתי הצורות של תסמונת Guillain-Barre, נוירופתיה אקסונלית מוטורית חריפה ופולינוירופטריה דלקתית חריפה (AIDP); זיהוי של אפיטופים DQ בטא הקשורים לרגישות והגנה מפני AIDP // J. אימונול. 2003. V. 170. P. 3074–3080. 16. Geleijns K., Schreuder G. M., Jacobs B. C. et al. אללים מסוג HLA II אינם גורם רגישות כללי בתסמונת Guillain-Barre // נוירולוגיה. 2005. ו' 64. עמ' 44–49. 17. Asbury A. K., Cornblath D. R. Assessment of אבחון הקריטריונים הנוכחיים לתסמונת Guillain-Barre // Ann. נוירול. 1990. V. 27. S. 21–24.
מֵידָע
קיצורים בשימוש בפרוטוקול
| CIDP | Polyradiculoneuropathy דלקתי כרוני |
| PNP | פולינוירופתיה |
| NMSP | פולינוירופתיה מוטורית-חושית תורשתית |
| SGB | תסמונת גילאן-בארה |
| גֵיהִנוֹם | יתר לחץ דם עורקי |
| PNS | מערכת עצבים היקפית |
| CNS | מערכת העצבים המרכזית |
| MRI | הדמיה בתהודה מגנטית |
| PCR | תגובת שרשרת פולימראז |
| CSF | נוזל מוחי |
| ESR | קצב שקיעה של אריתרוציטים |
| איג | אימונוגלובולין |
| קצב לב | קצב לב |
| איידס | תסמונת כשל חיסוני נרכשת |
| EMG | אלקטרומיוגרפיה |
| ENMG | electroneuromyography |
| IVIG | אימונוגלובולין אנושי תקין למתן תוך ורידי |
| GC | גלוקוקורטיקואידים |
רשימת מפתחי פרוטוקולים עם נתוני הסמכה:
1. Kaishibayeva Gulnaz Smagulovna, מועמד למדעי הרפואה, JSC "האוניברסיטה הרפואית של קזחית להשכלה מתמשכת", ראש המחלקה לנוירולוגיה, תעודת "נוירופתולוג למבוגרים".
2. Zhumagulova Kulparam Gabibulovna, מועמדת למדעי הרפואה, תעודה "נוירופתולוגית למבוגרים מהקטגוריה הגבוהה ביותר", JSC "האוניברסיטה הרפואית של קזחית להשכלה מתמשכת", פרופסור חבר של המחלקה לנוירולוגיה.
3. Raykhan Yesenzhanovna Tuleutaeva, פרמקולוגית קלינית, מועמדת למדעי הרפואה, פרופסור של האקדמיה הרוסית למדעי הטבע, ראש המחלקה לפרמקולוגיה ורפואה מבוססת ראיות, האוניברסיטה הרפואית של מדינת Semey.
אינדיקציה שאין ניגוד עניינים:לא.
רשימת סוקרים:
דושאנובה ג.א. - דוקטור למדעי הרפואה, פרופסור, ראש המחלקה לנוירולוגיה, פסיכיאטריה ופסיכולוגיה של האקדמיה הפרמצבטית של דרום קזחסטן.
ציון התנאים לתיקון הפרוטוקול:תיקון הפרוטוקול 3 שנים מיום פרסומו וממועד כניסתו לתוקף או אם קיימות שיטות חדשות ברמת ראיות.
קבצים מצורפים
תשומת הלב!
- על ידי תרופות עצמיות, אתה יכול לגרום נזק בלתי הפיך לבריאות שלך.
- המידע המתפרסם באתר MedElement אינו יכול ולא אמור להחליף ייעוץ רפואי אישי. הקפד לפנות למוסדות רפואיים אם יש לך מחלות או תסמינים שמטרידים אותך.
- יש לדון בבחירת התרופות והמינון שלהן עם מומחה. רק רופא יכול לרשום את התרופה הנכונה ואת המינון שלה, תוך התחשבות במחלה ובמצב גופו של החולה.
- אתר MedElement הוא משאב מידע והתייחסות בלבד. אין להשתמש במידע המתפרסם באתר זה לשינוי שרירותי של מרשמי הרופא.
- עורכי MedElement אינם אחראים לכל נזק בריאותי או נזק מהותי הנובע מהשימוש באתר זה.
תסמונת Guillain-Barré היא קבוצה של מחלות אוטואימוניות חריפות המתקדמת במהירות, שבהן ההתקף מכוון לתאי השואן ולמיאלין היוצרים את מעטפת סיבי העצב. התסמונת מתבטאת בפארזיס רפוי, הפרעות תחושתיות, הפרעות אוטונומיות. זה מתפתח 1 עד 3 שבועות לאחר זיהום במערכת העיכול או בדרכי הנשימה, ולכן מאמינים שהתגובה האוטואימונית מופעלת במקרים מסוימים על ידי מחלות עבר. התסמונת גורמת לסיבוכים קשים שבעבר היו קטלניים. אבל הודות לשיטות מודרניות לטיפול נמרץ, התמותה ירדה ל-5%.
הסיבות
הגורמים המדויקים לתסמונת Guillain-Barré לא הוכחו, אך קיימות מספר השערות למקור המחלה.
- פגיעה מוחית טראומטית. נזק פיזי מוביל לנפיחות של המוח ולהופעת גידולים בו. התסמונת עשויה להיות תוצאה רחוקה מכך, לכן האבחנה לוקחת בחשבון TBI באנמנזה.
- הַדבָּקָה. חולים רבים מציגים סימנים של זיהום בדרכי הנשימה ובמערכת העיכול 1 עד 3 שבועות לפני הופעת הסימפטומים של התסמונת. לכן, סביר להניח שהמחלה המועברת מעוררת תגובה אוטואימונית. בהיבט זה, התפקיד הפתולוגי מוקצה ל-Campylobacter jejuni, הגורם לדלקת מעיים, נגיפי הרפס, מיקופלזמה, Haemophilus influenzae, זיהום ב-HIV. התערבויות כירורגיות, חיסון, פציעות של עצבים היקפיים יכולים למלא תפקיד דומה.
- נטייה תורשתית. חולים שבמשפחתם ישנם מקרים של התסמונת נופלים לאזור הסיכון. עם תורשה מחמירה, גם פגיעת ראש וגם מחלות זיהומיות משמשות לעתים קרובות כגורם מעורר.
מִיוּן
בהתאם לתסמינים ולאזור המושפע, תסמונת Guillain-Barré יכולה ללבוש צורה קלאסית, אקסונלית, לא טיפוסית, או להתבטא כתסמונת מילר-פישר.
הצורה הקלאסית נצפית ב-80% מהמקרים והיא פוליראדיקולונורופתיה דלקתית-דמיאלינטית. הצורה האקסונלית מופיעה ב-15% מהמקרים, איתה קיימת נוירופתיה מוטורית או מוטורית-חושית עם פגיעה באקסונים של סיבי העצבים האחראים על התנועה והרגישות של השרירים. עם תסמונת מילר-פישר, הנצפית ב-3% מהמקרים, יש שיתוק בשרירי העין, היעדר רפלקס אחד או יותר, פארזיס קל ופגיעה בקואורדינציה ובמיומנויות המוטוריות. בצורה הלא טיפוסית, שהיא נדירה ביותר, יש נוירופתיה חושית ואוטונומית, כמו גם פולינוירופתיה גולגולתית.
על פי משך תקופת התסמינים המתגברים, התסמונת מחולקת לצורה חריפה (7-14 ימים), תת-חריפה (15-28 ימים) וכרונית (עד מספר חודשים עם תקופות של הפוגה והידרדרות). האחרון נחשב לחמור ביותר, שכן קשה יותר לאבחן אותו ומפחית את הסיכויים לטיפול בזמן.
תסמינים
התסמינים של תסמונת Guillain-Barré דומים בתחילה לאלה של זיהום נגיפי בדרכי הנשימה. טמפרטורת הגוף עולה בחדות, נצפית דלקת של דרכי הנשימה העליונות, המטופל מרגיש חולשה כללית ומפרקים כואבים. לפעמים מציינים הפרעות במערכת העיכול.
התסמונת שונה מ-ARVI בחולשה של הגפיים, ירידה ואובדן רגישות. בתחילה, אי נוחות מופיעה ברגליים התחתונות, ואז מתפשטת לכפות הרגליים, משפיעה על בהונות הרגליים. יש עקצוצים במפרקי האצבעות, וכאבים כואבים מתחלפים בחוסר תחושה. ככל שהמחלה מתקדמת, השליטה על תנועות פשוטות קטנות אובדת, למשל, קשה לכתוב ביד. התסמינים מופיעים באופן סימטרי בגפיים.
סימן אופייני נוסף הוא עלייה ניכרת בבטן. בשל העובדה שהנשימה נבנית מחדש לחלוטין מהסוג העליון לבטן, הבטן בולטת קדימה בצורה ניכרת. הדיאפרגמה נחלשת, קשה יותר ויותר לנשום עם הריאות.
כאשר שרירי הלוע מעורבים בתהליך הפתולוגי, היחלשותם מונעת בליעה תקינה. החולה עלול להיחנק מהרוק של עצמו. עקב היחלשות שרירי הפה, קשה לו ללעוס ולאכול. בגלל התסמונת, למטופל יש שליטה גרועה באצירת שתן ובגזים במעיים. התסמונת משפיעה כמעט על כל האיברים הפנימיים, וגורמת לטכיקרדיה, יתר לחץ דם, ראייה מטושטשת וביטויים נוספים.
הסימפטומים של תסמונת Guillain-Barré מחמירים לרוב במשך מספר שבועות. הכל מתחיל בחולשה קלה בגפיים ומוביל להפרעות בולטות. זה כרוך באבחון בטרם עת ובסיבוכים בעתיד. בצורה החריפה של המחלה, שיתוק יכול לכסות את רוב הגוף לאחר יום. בתחילה יש עקצוצים בגפיים, חולשה בכתפיים, בגב, באגן. קושי ברור בנשימה נרשם לאחר מספר שעות. יש לקחת את החולה בדחיפות למתקן רפואי שבו ניתן לעזור לו, כולל חיבור למכונת הנשמה.
ללא טיפול, התסמונת מובילה לסיבוכים בהם הסיכון למוות גבוה. זהו שיתוק של שרירי קבוצות הנשימה והבולבר, שרירי העיניים, הסרעפת, הבטן, הגב, כמו גם דלקת ריאות, תרומבואמבוליזם, דום לב, אלח דם.
אבחון
אבחון התסמונת כולל נטילת אנמנזה (תסמינים נוכחיים, פציעות אחרונות, SARS, הפרעות במערכת העיכול, חיסון משחקים תפקיד גדול). מתבצעת בדיקה נוירולוגית לאיתור הפרעות תחושתיות ותנועה וכן בדיקות מעבדה (סרולוגיה, בדיקות דם ושתן כלליות וביוכימיות).
אם יש חשד לתסמונת, יש לציין מחקר של נוזל המוח השדרתי על ידי ניקור מותני או עורף. אם מתגלה ריכוז חלבון גבוה (3-5 גרם/ליטר), הדבר מאשר את האבחנה. במקרים חמורים של המחלה, מתבצע מעקב אחר עבודת מערכת הלב וכלי הדם ומערכת הנשימה.
לתסמונת עשויים להיות סימנים דומים לפורפיריה, בוטוליזם, שבץ איסכמי, מיאסטניה גרביס, פוליו, מחלת מוח, שיתוק הנגרם על ידי אנטיביוטיקה. האבחנה של "תסמונת גילאן-בארה" נדחית אם הפארזה א-סימטרית, ההפרעות הן תחושתיות בלבד, יש הפרעות מתמשכות או חמורות באגן, אם יש היסטוריה של דיפתריה לאחרונה, הזיות, אשליות או הרעלה מוכחת עם מתכת כבדה. מלחים.
יַחַס
תסמונת Guillain-Barré מטופלת במסגרת בית חולים. המטופל זקוק לטיפול הולם, ניטור חומרה, טיפול תרופתי, במקרים מסוימים ניתוח דחוף.
טיפול תרופתי מכוון לעצירת התגובה האוטואימונית. לחולה מוצגים אימונוגלובולינים מסוג G, הניתנים תוך ורידי. יש להם תופעות לוואי כמו בחילות, חום וכאבי ראש, אך משפרים את תפקוד הנשימה. מבוצעת גם פלזמה ממברנה, שבה פלזמת הדם של המטופל מוחלפת בתמיסת כלוריד או בפריפולינוקין. זה מפחית את חומרת הפרזיס ומפחית את זמן התמיכה של המטופל במכשיר ההנשמה.
מטיפול סימפטומטי בתסמונת Guillain-Barré, נקבעים ויטמינים מקבוצת B, אנטי-היסטמינים, תרופות להורדת חום ומשככי כאבים, מווסתי דופק ולחץ, תרופות אנטי-טרומבוטיות ואנטיכולינאסטראזות ודמעות מלאכותיות.
עם הפרעות בולבריות ממושכות והתפתחות של כשל נשימתי, תיתכן ניתוח קנה הנשימה או הגסטרוסטום. חולשה ושיתוק של שרירי הנשימה והבולבר דורשים ניטור של פעילות הנשימה, קצב הלב ולחץ הדם. לעיתים יש צורך בקוצב לב, עם ירידה בקיבולת הריאות ב-25-30%, יש לציין שימוש במכשיר הנשמה. שיתוק בולברי מצריך החדרה של צינור אף. ייתכן שתצטרך גם להכניס קטטר לשלפוחית השתן שלך.
הטיפול בחולה כולל מניעת סיבוכים הקשורים לחוסר תנועה (פצעי לחץ, פקקת וכו'). לשם כך, המיקום של הגוף של המטופל משתנה כל שעתיים. ניקוי העור, התעמלות פסיבית, שליטה בעבודת המעיים ושלפוחית השתן נקבעים.
שיקום
הפרוגנוזה של המחלה חיובית בדרך כלל: 70% מהחולים מחלימים לחלוטין, ל-15% יש פרזיס ושיתוק, שבהם החולה מוכר כנכה. ב-5% מהמקרים המחלה עלולה להיות קטלנית, הסיכון מוגבר בילדים ובקשישים.
כ-2-5% מהמקרים קשורים למעבר של הצורה החריפה של המחלה למחלה חוזרת כרונית. לכן, חשוב לא רק לעקוב אחר כל המלצות הרופא, אלא גם לעשות מאמצים בשלב השיקום. עם תסמונת Guillain-Barré, זה יכול לקחת מספר חודשים או שנים. המטופלים לומדים ללכת שוב, להשתמש בסכו"ם, בכלי כתיבה. אמצעי שיקום כוללים עיסוי, תרגילים טיפוליים, מקלחות ניגודיות, אמבטיות עם ראדון ומימן גופרתי, טיפול באוזוצריט, אמבטיות פרפין, אלקטרופורזה, מגנטותרפיה, תזונה עם תכולה גבוהה של ויטמינים B, סידן, מגנזיום ואשלגן.
חולה שעבר את התסמונת צריך לעבור באופן קבוע אלקטרו-נוירומיוגרפיה כדי להעריך את הדינמיקה של המצב. כמו כן, יש צורך בבדיקות אצל נוירולוג, מה שיפחית את הסיכון להישנות. תוך 12 חודשים מהופעת המחלה אסור לחסן.
הירשמו לתור לרופא
Piradov M.A. 2000
אפשרי שיקום
למחלה זו יש לפחות שמונה שמות שונים - תסמונת לנדרי (על שם הנוירולוג הצרפתי שתיאר אותה לראשונה ב-1859), תסמונת Guillain-Barré-Stroll (מדענים שתרמו תרומה משמעותית לחקר המחלה), דלקת פוליראדיקולונאוריטיס חריפה וכו'. כיום על פי הסיווג הבינלאומי של מחלות, היא נקראת רשמית תסמונת Guillain-Barré (GBS) או פולינורופתיה פוסט-זיהומית חריפה. בנוירולוגיה, GBS נחשבת למחלה ייחודית. ולא כל כך בגלל הנדירות היחסית שלו (מתרחשת ב-2 אנשים לכל 100 אלף מהאוכלוסייה), אלא בגלל האפשרות לשיקום מלא של החולה, אם כי לפעמים חומרת נזקי ה-GBS דומה למחלות הקשות ביותר. סגן המנהל למדע של מכון המחקר לנוירולוגיה של האקדמיה הרוסית למדעי הרפואה, ראש המחלקה לנוירוריאנימציה, פרופסור מיכאיל PIRADOV מספר עוד. תסמונת Guillain-Barré היא הגורם השכיח ביותר לטטרפרזיס היקפי חריף ושיתוק. תסמינים נוירולוגיים מתפתחים מהר מאוד, בעוד שלא רק תפקודים מוטוריים, אלא גם תחושתיים (בעיקר רגישות מפרקים-שרירים) מופרים, ולעיתים באופן גס מאוד, ורפלקס הגידים פוחת עד להכחדה מוחלטת. הפרעות באגן אינן אופייניות ל-GBS, אך בשליש מהמקרים, שרירי הנשימה והבליעה נפגעים קשות. במקרים חמורים מופיע לפני הרופא אדם שוכב ללא תנועה במיטה, שאינו יכול לנשום כלל, לבלוע ואף לפקוח את עיניו. אבל אם לוקחים אלקטרואנצפלוגרמה ממטופל, היא תהיה זהה לזו של אדם בריא, וכאדם הוא לא השתנה ולו במעט מבחינה אינטלקטואלית. ב-70 אחוז. מקרים של GBS מתרחשים מספר ימים לאחר הופעת תסמינים דמויי שפעת: חום קל, כאבי שרירים, נזלת - כל מה שנקרא בדרך כלל זיהומים חריפים בדרכי הנשימה. בערך 15 אחוז. במקרים, התסמונת מופיעה לאחר שלשולים רבים, ב-5 אחוזים. - לאחר מניפולציות כירורגיות, בין אם מדובר בהפלות, כריתת herniotomy, כריתת תוספתן או ניתוחים מורכבים יותר. לעיתים המחלה מתפתחת לאחר סוגים שונים של חיסונים. GBS מתרחש בכל חלק של העולם, בכל עת של השנה, שכיח באותה מידה בשני המינים. הגיל הממוצע ברוב התצפיות הוא כ-40 שנה. יחד עם זאת, מבחינים בשני שיאי גיל קטנים: בגיל 20-25 ומעל גיל 60. במקרים קלאסיים, האבחנה של GBS פשוטה וכוללת שני סימנים מחייבים: הגברת חולשת השרירים בשתי גפיים לפחות וירידה משמעותית עד לאובדן מוחלט של רפלקסים בגידים. קריטריונים אבחוניים נוספים הם ירידה במהירות הולכת הדחף העצבי דרך השרירים עם היווצרות בלוק הולכה ופירוק תאי חלבון בנוזל השדרה. תסמונת Guillain-Barré מבוססת על מנגנונים אוטואימוניים, כאשר תפקידו של הגורם המעורר מוקצה לוירוסים וחיידקים מסוימים. עם זאת, עדיין אין חוות דעת סופית על אופי האנטיגן או האנטיגנים הגורמים להתפתחות של תגובות חיסוניות מפל. בחמש השנים האחרונות, הוכח כי מגוון שלם של פולינורופתיות משולבות בשם GBS: פולינורופתיה דלקתית דלקתית חריפה (מופיעה ב-75-80 אחוז מהמקרים); נוירופתיה מוטורית חריפה וכגרסה שלה, נוירופתיה אקסונלית מוטורית-חושית חריפה (15-20 אחוז); תסמונת פישר (3 אחוזים). רוב המחלות האוטואימוניות הן בלתי הפיכות. אבל עם GBS, התמונה שונה לחלוטין, ייחודית: המחלה מגבילה את עצמה. אם לחולה חולה קשה ניתן רק אוורור ריאות מלאכותי למשך מספר חודשים, העצבים הפגועים משוחזרים. ושלמה כמעט כמו בשימוש בשיטות המודרניות העיקריות לטיפול ב-GBS - פלזמהפרזה או טיפול תוך ורידי באימונוגלובולינים מסוג G. עלולה להתעורר השאלה: מדוע לטפל בחולה בשיטות יקרות? אבל תארו לעצמכם מה זה אומר להיות במכשיר הנשמה במשך 3-6 חודשים ולהיות מרותק למיטה? שימוש בזמן בפלזמפרזיס ובאימונוגלובולינים מסוג G יכול להפחית את הזמן המושקע באוורור מכני למספר שבועות ואפילו ימים, לשנות מהותית את מהלך ותוצאת המחלה. זה לא סוד שכיום בארץ חולים רבים עם צורות קשות של GBS מתים. הדבר נובע בעיקר מהעובדה שבתי חולים רבים אינם מצוידים בציוד נשימתי איכותי או שאין להם כוח אדם מוסמך לאוורור ריאות מלאכותי לטווח ארוך. חולים מתים עקב זיהומים בנאליים ופצעי שינה. בנוסף, רחוק מכל מקום ישנה אפשרות לבצע פעולות פלזמהזיס עם החלפת נפחים גדולים של פלזמה (עד 200 מ"ל פלזמה/ק"ג לקורס טיפול המורכב מ-4-5 פעולות). זה ממש לא מקובל לטפל בחולים כאלה בבית חולים כפרי או מחוז קטן - הם חייבים להתאשפז בבתי חולים גדולים יותר מצוידים במתקנים ובציוד הדרושים. טעות אופיינית במקרים רבים היא טיפול בחולים עם GBS בתכשירים הורמונליים: מחקרים מיוחדים של למעלה מאלף חולים הראו שההורמונים אינם משפיעים על קצב ההחלמה של תפקוד לקוי, אלא להיפך, נושאים סיבוכים רבים. עם זאת, הורמונים ממשיכים להיות בשימוש בלתי סביר אפילו במספר מרפאות בערים הגדולות ברוסיה. בחו"ל, בשביל זה, אפשר פשוט לשלול מהם רישיון רפואי. אם אנחנו מדברים על הצד הכספי של העניין, כמובן, כיום, עבור רוב החולים, טיפול באימונוגלובולינים מסוג G מיובאים, שנמצאים בשימוש נרחב במערב, הוא פשוט לא סביר, אלא, למרבה המזל, קורס של תוכנית פלזמהרזיס ב- המדינה שלנו הרבה יותר זולה. וההשפעה הטיפולית של שתי שיטות הטיפול הללו זהה: כ-85-90 אחוז. במקרים, אדם עם תסמונת גיליין-בארה, למרות הנזק החמור ביותר למערכת העצבים ההיקפית, מחלים לחלוטין, ורק 10-15 אחוזים. חולים חווים השפעות שיוריות. כמובן, השכיחות של תסמונת Guillain-Barré אינה ניתנת להשוואה לשבץ מוחי, פגיעה מוחית טראומטית או אפילפסיה. אבל עם שבץ, במקרה הטוב, 20 אחוז משוחזרים. אנשים, וטיפול בזמן של תסמונת Guillain-Barré עם לא פחות חומרת הנגע נותן השפעה הרבה יותר גדולה. ואם בכל שנה כ-200 אנשים סובלים מה-SSS רק במוסקבה, זה הרבה כדי לשקם את בריאותם של 180 אנשים. בתרגול שלי, היה מקרה שבו המחלה פגעה בבחור בן 18, מועמד לתואר אמן ספורט באתלטיקה: הוא לא יכול היה לנשום, לבלוע, לזוז בכוחות עצמו. שנה לאחר מכן, האיש הזה מילא את הסטנדרט של אמן ספורט. ויש הרבה דוגמאות כאלה - לאחר טיפול נכון ב-GBS, נשים צעירות יולדות ילדים, הרוב המכריע של החולים חוזרים לחיים מלאים.
מילים נרדפות: polyradiculo(נוירו)פתיה חריפה demyelinating, פולינורופתיה פוסט-זיהומית חריפה, תסמונת Landry-Guillain-Barré, מיושן. שיתוק עולה של לנדרי.
טווח תסמונת גילאן-בארההוא כינוי (כלומר מתן שם) לקבוצה של תסמונות פוליראדיקולונורופתיה דלקתיות חריפות אוטואימוניות המאופיינות בשיתוק רפוי סימטרי מתקדם בשרירי הגפיים והשרירים המועצבים על ידי עצבי גולגולת (עם התפתחות אפשרית של הפרעות נשימה ובליעה מסוכנות) עם או ללא הפרעות רגישות ואוטונומיות (לחץ דם לא יציב, הפרעות קצב וכו').
לעתים קרובות המחלה מתפתחת ישירות לאחר הזיהומים המועברים. בגרסה הקלאסית של התסמונת, נצפה (מהרגליים) טטרפרזיס (פרזיס (שיתוק) של כל ארבע הגפיים).
האבחנה נעשית על בסיס ניתוח של התמונה הקלינית האופיינית ומאושרת על ידי בדיקת נוזל מוחי ומחקר אלקטרומיוגרפי (EMG).
הטיפול בתסמונת Guillain-Barré מתבצע ביחידה לטיפול נמרץ בשליטה של תפקודי נשימה ובליעה. השיטות העיקריות של טיפול ספציפי הן פלזמהפרזה יעילה באותה מידה וטיפול בדופק תוך ורידי עם אימונוגלובולין G. התאוששות טובה בשרירים משותקים נצפית בכ-75-85% מהמקרים.
יחד עם העובדה שתסמונת גווילין-בארה מוצגת באופן קלאסי כפולינוירופתיה דה-מיילינציה עם חולשה עולה, הנקראת פולינורופתיה דלקתית דלקתית חריפה ומהווה 75-80% מהמקרים, תוארו וזוהו מספר וריאנטים או תת-סוגים לא טיפוסיים של תסמונת זו. ספרות, המייצגת קבוצה הטרוגנית של נוירופתיות פריפריות תלויות חיסונית: תסמונת מילר-פישר (3 - 5%), פולינורופתיה אקסונלית מוטורית חריפה ופולינוירופתיה אקסונלית סנסומוטורית חריפה (מרכיבות 15-20%), ולעיתים רחוקות יותר פולינורופתיה חושית חריפה, פנדיאוטונומיה חריפה. , פולינורופתיה גולגולתית חריפה, אפשרות לוע-צוואר הרחם-ברכיאלית. ככלל, וריאנטים אלה בדרך כלל קשים יותר מבחינה קלינית מהעיקרי.
- אֶפִּידֶמִיוֹלוֹגִיָה
תסמונת Guillain-Barré היא הפולינוירופתיה החריפה השכיחה ביותר. השכיחות היא 1.7 - 3.0 לכל 100,000 אוכלוסייה בשנה, שווה בקירוב בקרב גברים ונשים, אין תנודות עונתיות, והיא שכיחה יותר בגיל מבוגר. השכיחות בגיל 15 שנים היא 0.8 - 1.5, ובגיל 70 - 79 שנים היא מגיעה ל-8.6 ל-100,000. התמותה נעה בין 2 ל-12%.
- קוד ICD-10 G.61.0
יַחַס
- נקודות מפתח
- הטיפול בתסמונת Guillain-Barré כולל שני מרכיבים: טיפול תומך לא ספציפי וטיפול ספציפי בפלזמהפרזה או טיפול בדופק עם אימונוגלובולינים מסוג G.
- בשל האפשרות לפתח דקומפנסציה עם אי ספיקת נשימה חמורה תוך מספר שעות, כמו גם הפרעות קצב לב, יש צורך לטפל בתסמונת Guillain-Barré בשלב החריף כמצב חירום. במקרים של התפתחות אי ספיקת נשימה חריפה במוסד רפואי, חייבת להיות אפשרות לערוך אוורור מלאכותי לטווח ארוך של הריאות.
- במקרים חמורים עם התפתחות מוקדמת של כשל נשימתי חריף, הטיפול מתבצע ביחידה לטיפול נמרץ או ביחידה לטיפול נמרץ. מתבצע ניטור שעתי של VC, גזי דם, אלקטרוליטים בדם, קצב לב, לחץ דם, מצב השרירים הבולבריים (הופעה והגברה של הפרעות בליעה שאינן מביאות להקלה בשיעול, צרידות, הפרעות דיבור). עם שיתוק בולברי עם הפרעות בליעה, חנק, מזיגת המשקה דרך האף, יש לציין החדרה של צינורית nasogastric, ולעיתים קרובות אינטובציה (למניעת דלקת ריאות שאיבה ושאיבה). אינטובציה של קנה הנשימה עם אוורור מכני מסומנת עם התפתחות של כשל נשימתי, אם ה-VC יורד מתחת ל-12-15 מ"ל/ק"ג, ועם שיתוק בולברי והפרות של בליעה ודיבור מתחת ל-15-18 מ"ל/ק"ג. בהיעדר נטייה לשחזר את הנשימה הספונטנית תוך שבועיים, מבוצעת טרכאוסטומיה.
- כרגע אין שימוש בקורטיקוסטרואידים מכיוון שהוכח שהם לא יעילים. הם אינם משפרים את תוצאות המחלה.
- טיפול ספציפי
טיפול ספציפי באמצעות פלזמפרזיס או מתן תוך ורידי של מינונים גבוהים של אימונוגלובולין מתחיל זמן קצר לאחר האבחנה. מוצגת יעילות שווה בערך של שתי שיטות הטיפול, כמו גם היעדר השפעה נוספת משילוב של שיטות אלה. נכון לעכשיו, אין הסכמה לגבי הבחירה בטיפול ספציפי.
בהתחשב בכך שקיימת סבירות גבוהה להחלמה ספונטנית, הטיפול בחולים עם תסמונת Guillain-Barré קלה יכול להיות מוגבל לטיפול לא ספציפי ותומך. עם חומרה מתונה של התהליך, ובמיוחד במקרים חמורים, טיפול ספציפי מתחיל מוקדם ככל האפשר.
לטיפול באימונוגלובולין יש יתרון מסוים על פני פלזמפרזיס, שכן הוא קל ונוח יותר לשימוש, בעל מספר נמוך משמעותית של תופעות לוואי, קל יותר למטופל, ולכן אימונוגלובולין הוא התרופה המועדפת בטיפול בתסמונת Guillain-Barré. .
- טיפול בדופק תוך ורידי עם אימונוגלובוליןטיפול בדופק תוך ורידי עם אימונוגלובולין (IgG, תכשירים - אוקטגאם, סנדוגלובולין, אינטראגלובולין, אימונוגלובולין אנושי תקין) מיועד לחולים שאינם מסוגלים ללכת יותר מ-5 מ' ללא סיוע, או חמורים יותר (עם שיתוק, הפרעות נשימה ובליעה) עם מקסימום יעילות התרופה בתחילת הטיפול תוך 2 עד 4 שבועות מתחילת המחלה. זה ניתן לווריד במינון של 0.4 גרם / ק"ג ליום למשך 5 ימים (מנה כוללת של 2 גרם / ק"ג או כ-140 גרם). סכימה חלופית למתן מינון זהה: 1 גרם / ק"ג ליום בשתי מנות למשך יומיים. השימוש בו מוגבל על ידי העלות הגבוהה שלו.
- פלזמפרזיספלזמפרזיס הניתנת בשלב התקדמות המחלה (בערך בשבועיים הראשונים) כמעט מכפילה את תהליך ההחלמה ומפחיתה את הפגם הנותר. זה נקבע במקרים מתונים וחמורים על פי תכנית של 4 - 6 מפגשים כל יומיים, עם החלפה של 50 מ"ל / ק"ג לכל מפגש (לפחות 35-40 מ"ל פלזמה לק"ג משקל גוף), בסך הכל עבור הקורס כולל 200 - 250 מ"ל / ק"ג (לפחות 160 מ"ל פלזמה לכל ק"ג משקל גוף לכל קורס). במקרים קלים ובשלב ההחלמה, פלזמפרזיס אינה מותאמת. פלזמפרזיס הראתה יעילות גבוהה למדי כאשר ניתנה לחולים חולים קשים, כאשר הטיפול החל יותר מ-30 יום לאחר הופעת המחלה.
ב-5-10% מהחולים מתרחשת הישנות המחלה לאחר סיום הטיפול בפלזמפרזיס או אימונוגלובולין. במקרה זה, המשך טיפול באותה שיטה, או השתמש בשיטה חלופית.
- טיפול ושיקום לא ספציפיים
- יש צורך למנוע פקקת ורידים עמוקים של הרגל התחתונה בחולים מרותקים למיטה (במיוחד עם שיתוק ברגליים). נוגדי קרישה של פנילין או וורפרין בפעולה עקיפה ניתנים דרך הפה במינונים המייצבים את ה-INR ברמה של 2.0, או פרקסיפרין (נדרופארין) 0.3 מ"ל. s/c 1 - 2 פעמים ביום, או sulodexide (Wessel Due F) 2 פעמים ביום, 1 אמפולה (600 LSU) / m למשך 5 ימים, ולאחר מכן דרך הפה 1 כובעים (250 LSU) 2 פעמים ביום. המניעה מתבצעת לפני הזמן שבו המטופל מתחיל לקום מהמיטה. אם התפתחה פקקת לפני תחילת הטיפול, טיפול מניעתי מתבצע על פי אותה תכנית. כמו כן נעשה שימוש בחבישת תחבושת אלסטית של הרגליים לאמצע הירך (או משתמשים בגרביים עם דחיסה מדורגת) והרמת הרגליים ב-10-15º. מוצג פסיבי ובמידת האפשר אקטיבי "הליכה במיטה" עם כיפוף רגליים, פולט הליכה במשך 5 דקות 3-5 פעמים ביום.
- עם פרזיס של שרירי הפנים, ננקטים אמצעים להגנה על הקרנית: החדרת טיפות עיניים, רטייה לעין בלילה
- מניעת התכווצויות ושיתוק. לשם כך, תרגילים פסיביים מתבצעים 1-2 פעמים ביום, הם מבטיחים את המיקום הנכון במיטה (מיטה נוחה, תומכות כף הרגל), לעסות את הגפיים. לאחר מכן, תרגילי פיזיותרפיה פעילים מחוברים.
- מניעת פצעי שינה - החליפו תנוחה במיטה כל שעתיים, נגבו את העור בתרכובות מיוחדות, השתמשו במזרונים נגד דקוביטוס.
- מניעת זיהום בריאות בצורה של תרגילי נשימה, התגייסות מוקדמת ככל האפשר של המטופל. עם ירידה ביכולת החיוניות של הריאות, קושי בהפרדת הפרשות הסימפונות, מוצג עיסוי (מאמץ ורטט תוך הפיכת הגוף בשכיבה) כל שעתיים במהלך היום.
- טיפול סימפטומטי: אנטי-אריתמי, לחץ דם נמוך, משכך כאבים. עם תת לחץ דם עורקי, ירידה בלחץ הדם (בערך לחץ דם 100 - 110/60 - 70 מ"מ כספית ומטה), תמיסות קולואידיות או גבישיות ניתנות תוך ורידי (תמיסה איזוטונית של נתרן כלורי, אלבומין, פוליגלוקין), ובמקרה של אי ספיקה. השפעה בשילוב עם קורטיקוסטרואידים: פרדניזולון 120 - 150 מ"ג., Dexazone 8 - 12 מ"ג. במקרה של אי ספיקה של הכספים הללו, נעשה שימוש ב-vasopressors: דופמין (50 - 200 מ"ג. מדולל ב-250 מ"ל. תמיסת נתרן כלוריד איזוטונית וניתנת בקצב של 6-12 טיפות/דקה), או נוראדרנלין, או מזוטון. לכאב בינוני משתמשים במשככי כאבים פשוטים ובתרופות נוגדות דלקת לא סטרואידיות. בתסמונת כאב חמור משתמשים בטרמל או קבמזפין (טיגרטול) או גבפנטין (Neurontin), אולי בשילוב עם תרופות נוגדות דיכאון טריציקליות (אימיפרמין, אמיטריפטילין, אזפן וכו').
- שיעורים עם קלינאית תקשורת לטיפול ומניעה של הפרעות דיבור ובליעה.
- השיקום כולל עיסוי, תרגילים טיפוליים, פיזיותרפיה. גירוי שרירים דרך העור מתבצע לכאבי שרירים ולפרזה של הגפיים.
כל תוכן iLive נבדק על ידי מומחים רפואיים כדי להבטיח שהוא מדויק ועובדתי ככל האפשר.
יש לנו הנחיות קפדניות למקורות ומצטטות רק אתרים מוכרים, מכוני מחקר אקדמיים ובמידת האפשר מחקר רפואי מוכח. שימו לב שהמספרים בסוגריים (וכו') הם קישורים למחקרים מסוג זה.
אם אתה מאמין שתוכן כלשהו שלנו אינו מדויק, מיושן או מפוקפק בדרך אחרת, אנא בחר בו והקש Ctrl + Enter.
תסמונת Guillain-Barré (פולינוירופתיה אידיופטית חריפה; שיתוק של לנדרי; פוליראדיקולונורופתיה דלקתית חריפה) היא פולינורופתיה דלקתית חריפה, בדרך כלל מתקדמת במהירות, המאופיינת בחולשת שרירים ואובדן קל של תחושה דיסטלית. מחלת כשל חיסוני. אבחון לפי נתונים קליניים. טיפול בתסמונת Guillain-Barré: plasmapheresis, y-globulin, לפי אינדיקציות אוורור מלאכותי של הריאות. תוצאת התסמונת משתפרת משמעותית עם טיפול תומך הולם ביחידה לטיפול נמרץ ושימוש בשיטות מודרניות של טיפול אימונומודולטורי.
, , , , , , ,
קוד ICD-10
תסמונת G61.0 Guillain-Barré
אֶפִּידֶמִיוֹלוֹגִיָה
השכיחות היא בין 0.4 ל-4 מקרים לכל 100,000 אוכלוסייה בשנה. תסמונת Guillain-Barré נצפית בכל קבוצות הגיל, אך לעתים קרובות יותר אצל אנשים בגילאי 30-50 שנים, בשכיחות שווה בקרב גברים ונשים. הבדלים גזעיים, גיאוגרפיים ועונתיים בשכיחות של תסמונת Guillain-Barré אינם אופייניים בדרך כלל, למעט אולי נוירופתיה אקסונלית מוטורית חריפה, הנפוצה ביותר בסין וקשורה בדרך כלל לזיהום במעיים עקב קמפילובקטר ג'יוניולכן לעתים קרובות יותר להתרחש בקיץ.
השכיחות עולה משמעותית לאחר גיל 40. תסמונת Guillain-Barré הורגת בממוצע 600 אנשים בשנה בארצות הברית. לפיכך, תסמונת Guillain-Barré היא בעיה בריאותית חשובה מאוד, רלוונטית במיוחד לקשישים.
, , , , ,
גורמים לתסמונת גילאן-בארה
הנוירופתיה הדלקתית הנרכשת הנפוצה ביותר. המנגנון האוטואימוני אינו מובן במלואו. ידועות מספר גרסאות: בחלקן, דה-מיאלינציה שולטת, באחרות האקסון סובל.
בכ-2/3 מהמקרים התסמונת מופיעה 5 ימים עד 3 שבועות לאחר מחלה זיהומית, ניתוח או חיסון. ב-50% מהמקרים המחלה קשורה לזיהום קמפילובקטר ג'ג'וני,נגיפי אנטרו ונגיפי הרפס (כולל ציטומגלווירוס ווירוסים הגורמים למונונוקלאוזיס), וכן Mycoplasma spp.בשנת 1975 הייתה התפרצות הקשורה לתוכנית החיסון נגד שפעת החזירים.
, , , , ,
פתוגנזה
דה-מיאלינציה וחדירה דלקתית בשורשי עצבי עמוד השדרה ובעצבים פרוקסימליים עשויים להסביר את ההצגה הקלינית של תסמונת Guillain-Barré. הוא האמין כי חסינות הומורלית ותאית מעורבים בפתוגנזה של המחלה. נוכחותם של לימפוציטים ומקרופאגים באזורים הפריווניים והאינטראקציה שלהם עם אקסונים בעלי מיאלינציה מצביעים בעיקר על התפקיד האפשרי של תגובות אוטואימוניות בתהליך הדמיילינציה. עמדה זו מאושרת על ידי תצפיות קודמות, לפיהן חיסון של חיות מעבדה עם מיאלין היקפי משולב גורם לדלקת עצבים אלרגית ניסיונית. למרות שחלבוני מיאלין מטוהרים - למשל, שברי חלבון בסיסי של מיאלין P2 או P2 פפטיד וחלבון PO - הוכחו מאוחר יותר כמסוגלים לגרום לנוירופתיה נסיונית, נוגדנים לתרכובות אלו נמצאים רק לעתים נדירות בתסמונת Guillain-Barré. תאי T מבודדים מהטחול ומבלוטות הלימפה של חולדות שחוסנו עם פפטיד סינתטי P2 53-78 יכולים לשחזר באופן ניסיוני דלקת עצבים אלרגית ניסיונית חמורה בעכברים סינגניים. לפיכך, מנגנוני חיסון תאיים ואולי גם הומורליים עשויים לתווך את יצירת מודל ניסיוני של נזק דלקתי לעצבים היקפיים.
מחקרים עדכניים משכו את תשומת הלב לתפקידם של גלוקו-קונגוגטים וליפופוליסכרידים של מעטפת המיאלין, קרום תאי שוואן או קרום אקסונלי כאנטיגנים העיקריים המתחילים את התגובה הדלקתית/אימונית בתסמונת Guillain-Barré. במחקר מפורט שנערך ביפן, התגלו אנטיגנים בחולים קמפילובקטר ג'יוני. במחקר זה נעשה שימוש בשיטת פנר לאיתור ליפופוליסכרידים עמידים בחום, ושיטת ליאור שימשה לאיתור אנטיגנים חלבוניים עמידים בחום. אנטיגנים PEN 19 ו-LIO 7 ג'ג'וניהיו מבודדים לעתים קרובות יותר בחולים עם תסמונת גיליין-בארה (בהתאמה, ב-52 ו-45% מהמקרים) מאשר בחולים עם דלקת מעיים ספוראדית הנגרמת על ידי ג'ג'וני(בהתאמה 5 ו-3%), והיו קשורים לעלייה בטיטר של נוגדנים ל-GM1 (ייתכן בגלל נוכחות של אנטיגן ליפופוליסכריד דמוי GML). על פי דיווחים ממדינות אחרות, הזיהום ג'ג'וניהרבה פחות סיכוי להקדים את הפיתוח של GBS. בנוסף, אחוז החולים עם נוגדנים אנטי-גנגליוסידים היה משתנה הרבה יותר, ונע בין 5% ל-60%. בנוסף, לא נמצא מתאם בין נוכחות נוגדנים ל-GM1 לבין הביטויים הקליניים והאלקטרופיזיולוגיים של המחלה.
בתסמונת מילר פישר, לעתים קרובות מתגלים נוגדנים ל-GQlb. באמצעות שיטות אימונוהיסטוכימיות, GQlb זוהה באזור הפרנודלי של עצבי הגולגולת האנושיים המעצבבים את העיניים. נמצא כי נוגדנים אנטי-GQlb יכולים לחסום העברה במערכת העצבית-שרירית של עכברים.
בגרסה המוטורית האקסונלית של תסמונת Guillain-Barré, קדמה למחלה לעתים קרובות יותר הידבקות ב-C. jejuni, ונוגדנים ל-GM1 ganglioside ולמוצר הפעלת המשלים C3d היו קשורים לאקסולמה של סיבים מוטוריים.
נוגדנים נגד GMI יכולים גם להיקשר לצמתים של Ranvier, ובכך לשבש את הולכת הדחפים. בנוסף, נוגדנים אלו מסוגלים לגרום לניוון של קצוות סיבים מוטוריים ואקסונים תוך-שריריים, אשר הוכח לאחרונה בחולים עם פולינורופתיה אקסונלית מוטורית חריפה. דלקת מעיים הנגרמת על ידי C. jejuni יכולה לעורר את תסמונת Guillain-Barré על ידי הגברת ייצורם של לימפוציטים מסוג T Gamma-delta שיכולים להשתתף באופן פעיל בתהליכים דלקתיים/חיסונים. רמות גבוהות בסרום של tumor necrosis factor-alpha (TNF-a), אך לא interleukin-1b או קולטן interleukin-2 מסיס, נמצאות בקורלציה לשינויים אלקטרו-פיזיולוגיים בתסמונת Guillain-Barré. בדיקה של דגימות נתיחה מצביעה על כך שלפחות בחלק מהמקרים של הצורה הדלקתית החריפה הקלאסית של תסמונת Guillain-Barré, משלים מעורב - הדבר מצוין על ידי זיהוי של רכיבי C3d ו-C5d-9 על פני השטח החיצוניים של תאי שוואן שנוצרים. קומפלקס התקפי קרום.
לפיכך, רוב המרכיבים המעורבים בדרך כלל בפתוגנזה של מחלות בתיווך חיסון נמצאים בתסמונת Guillain-Barré. למרות שסביר להניח שנוגדנים אנטי-גלוקו-מצומדים מעורבים בפתוגנזה של מספר צורות קליניות שונות של תסמונת Guillain-Barré, תפקידם המדויק אינו ידוע. גם אם קיימים נוגדנים ל-GM1, הם יכולים להיקשר לא רק ל-GM1, אלא גם לגליקוליפידים או גליקופרוטאין אחרים שיש להם אתרי פחמימות דומים. בהקשר זה, האנטיגנים הספציפיים של תאי שוואן או הממברנה האקסונלית שנגדה מכוונת התגובה הדלקתית/אימונית, כמו גם התפקיד האפשרי של אימונוגלובולינים, דורשים בירור. יתרה מכך, במקרים רבים של תסמונת Guillain-Barré, אין עדות לזיהום קודם או במקביל. ג'ג'וני,נוגדנים ל-GM1 או תכונות של מיקרואורגניזם אחר שאנטיגנים שלו יכולים ליזום תגובה חיסונית (לדוגמה, באמצעות חיקוי מולקולרי).
המחקר של חומרים המתקבלים מביופסיית עצבים ומנתיחה שלאחר המוות מראה שגם מנגנוני חיסון תאי תורמים להתפתחות תסמונת גיליין-בארה. במקרים חמורים של תסמונת Guillain-Barré, לימפוציטים ומקרופאגים נמצאים בכל הסיבים המוטוריים מהשורשים ועד הקצוות, ומקרופאגים פעילים נמצאים במגע הדוק עם מיאלין או פגוציזים את המיאלין. למרות שהתקבלו נתונים במודל ניסיוני של נוירופתיה דלקתית המאששים את מעורבותם של לימפוציטים מסוג T בנזק עצבי, אין הוכחות משכנעות לכך שהדבר מתרחש בחולים עם תסמונת Guillain-Barré. נתונים שהצטברו עד כה תומכים במעורבות של לימפוציטים מסוג T פעילים שחוצים את מחסום הדם-מוח ומתחילים דה-מיילינציה יחד עם נוגדנים לאנטיגנים ספציפיים של סיבי עצב, ציטוקינים (כגון TNF-a ואינטרפרון-y), רכיבים משלימים, אולי כולל קומפלקס תקיפת ממברנה ומקרופאגים מופעלים. . יש צורך במחקר נוסף כדי להבהיר את התפקיד של כל אחד מהאלמנטים הללו, כמו גם את הרצף שבו הם מעורבים בפתוגנזה של תסמונת Guillain-Barré.
, , , , , , , , , , ,
תסמינים של תסמונת גילאן-בארה
תסמינים של תסמונת Guillain-Barré הם הדומיננטיות של paresis רפוי (כמה שיותר פרוקסימלי, יותר עמוק), הפרעות רגישות פחות בולטות. בדרך כלל, חולשה כמעט סימטרית עם paresthesias מתחילה ברגליים, לעתים רחוקות יותר בזרועות או בראש. ב-90% מהמקרים החולשה מגיעה למקסימום בשבוע ה-3 למחלה. אובדן רפלקסים עמוקים בגידים. תפקוד הסוגרים נשמר. במקרים חמורים, חולשה של שרירי הפנים והפה-לוע בולטת במחצית מהמקרים. ב-5-10% מהמקרים נדרשת אינטובציה ואוורור מכני עקב שיתוק שרירי הנשימה.
לפעמים (כנראה, עם צורה וריאנטית), מתפתחת חוסר תפקוד אוטונומי בולט עם תנודות בלחץ הדם, הפרשה חריגה של הורמון אנטי-דיורטי, הפרעות קצב, קיפאון מעיים, אצירת שתן ותגובת אישונים לקויה לאור. תסמונת פישר היא גרסה נדירה של תסמונת Guillain-Barré וכוללת אופתלמופלגיה, אטקסיה וארפלקסיה.
הסימפטומים הראשונים, סדר הופעתם והדינמיקה שלהם
בדרך כלל, תסמונת Guillain-Barré מתחילה בחולשת שרירים ו/או הפרעות תחושתיות (חוסר תחושה, פרסטזיה) בגפיים התחתונות, שמתפשטות לגפיים העליונות לאחר מספר שעות או ימים.
התסמינים הראשונים של Guillain-Barré הם הפרעות תחושתיות, כגון paresthesias בכפות הרגליים. למרות שסימנים אובייקטיביים של ליקוי חושי שכיחים, הם בדרך כלל קלים. ביטויים מוקדמים ולא נעימים ביותר של המחלה לחולים יכולים להיות כאבים כואבים עמוקים בגב ודיססתזיה כואבת בגפיים. שיתוק עשוי לערב בתחילה את הגפיים התחתונות ולאחר מכן להתפשט במהירות כלפי מעלה על פני מספר שעות או ימים לגפיים העליונות, לחקות, לשרירי הנשימה ולנשימה. עם זאת, תיתכן גם התפתחות נוספת של אירועים, כאשר המחלה מתחילה בחולשה בשרירים המחקים ובגפיים העליונות, ואז מערבת את הגפיים התחתונות. כבר מההתחלה, הסימפטומים הם בדרך כלל סימטריים, והשיתוק מלווה באובדן או היחלשות של הגיד והרפלקסים הפריוסטאליים. סיבים אוטונומיים מעורבים לעתים קרובות בתסמונת Guillain-Barré. תסמינים אוטונומיים מתגלים בכ-50% מהמקרים, אך תפקוד הסוגר לרוב אינו מושפע. למחלה מהלך מונופאזי: תקופה של התגברות התסמינים הנמשכת מספר ימים או שבועות גוררת אחריה תקופת מישור הנמשכת בין מספר ימים למספר חודשים, ולאחריה מתרחשת החלמה על פני מספר חודשים. בשנים 1976-1977 חלה עלייה קלה בשכיחות של תסמונת Guillain-Barré הקשורה לחיסון בחיסון נגד שפעת החזירים, אך לא נרשמה תופעה דומה עם חיסון בגרסה אחרת של חיסון השפעת בשנים 1980-1988.
במקרים קלאסיים, המתבטאים בשילוב של תסמינים מוטוריים, תחושתיים ואוטונומיים, המבוססים על פוליראדיקולונורופתיה דה-מיילינציה, האבחנה של תסמונת Guillain-Barré היא לעתים נדירות קשה. עם זאת, יש גם גרסה אקסונלית של תסמונת Guillain-Barré, המתבטאת בעיקר בהפרעות מוטוריות ונוירופתיה אקסונלית מוטורית-חושית חריפה. הצורה האקסונלית החריפה מופיעה בדרך כלל עם פגם תפקודי חמור יותר ויש לה פרוגנוזה גרועה יותר. השילוב של אופתלמופלגיה, אטקסיה וארפלקסיה אופייני לגרסה אחרת של תסמונת גיליין-בארה, המכונה תסמונת מילר פישר. מנקודת מבט אבחנתית, בהיעדר תסמינים של פגיעה בעצב הגולגולת, אפילו עם תפקוד שלם של הסוגר, יש צורך לשלול את דחיסת חוט השדרה באמצעות הדמיה עצבית. באבחנה המבדלת חשוב לזכור גם פורפיריה חריפה לסירוגין, שיכרון מתכת שעלול לגרום לפולינוירופתיה חריפה וכן מחלות מערכתיות כמו מונונוקלאוזיס זיהומיות, תסמונות פרנפלסטיות או הפרעות מטבוליות שונות. חולים נגועים ב-HIV נוטים לפתח פולינוירופתיה או פוליראדיקולונורופתיה, אשר עשויה להיות קשורה לתסמונת Guillain-Barré, Cytomegalovirus polyradiculoneuropathy או לימפומה. קשה להבדיל מצבים אלו על סמך הצגה קלינית בלבד, אך בדיקת נוזל מוחי בפוליראדיקולונורופתיה הקשורה ל-HIV מגלה בדרך כלל פליאוציטוזיס נויטרופילי ועדויות לשכפול ויראלי.
חוסר תפקוד אוטונומי (כולל הפרעות לינה, כאבי בטן וחזה, יתר לחץ דם עורקי, טכיקרדיה) עלולים להחמיר משמעותית את מצבו של המטופל ולשמש סימן פרוגנוסטי לא חיובי. במחקר אחד, סימנים תת-קליניים למעורבות של מערכת העצבים הסימפתטית והפאראסימפתטית, שזוהו על ידי בדיקות לתפקודים אוטונומיים, תועדו ברוב המוחלט של החולים.
סולם חומרת הליקויים המוטוריים בצפון אמריקה
- שליש מהחולים מפתחים אי ספיקת נשימה.
- ברוב המקרים קיימות הפרעות של רגישות שטחית בצורת היפו-אסתזיה קלה או בינונית מהסוג הפולינויריטי (כמו "גרביים וכפפות"). לעתים קרובות ציין כאב באזורי הירכיים, המותניים והעכובים. הם יכולים להיות נוציספטיביים (שריריים) או נוירופתיים (עקב נזק לעצבים תחושתיים). הפרעות של רגישות עמוקה (במיוחד רטט ותחושת שרירים-מפרקים), שהן קשות מאוד (עד אובדן מוחלט), מתגלות בכמחצית מהחולים.
- נגעים בעצב הגולגולת נראים ברוב החולים. אפשר לערב כל עצב גולגולתי בתהליך (למעט זוגות I ו-II), אך התבוסה של זוגות VII, IX ו-X נצפית בעקביות הגדולה ביותר, המתבטאת בפארזה של שרירי הפנים והפרעות בולבריות. .
- הפרעות אוטונומיות נצפות ביותר ממחצית מהחולים ויכולות להיות מיוצגות על ידי ההפרעות הבאות.
- יתר לחץ דם עורקי חולף או מתמשך או תת לחץ דם עורקי לעתים רחוקות יותר.
- הפרעות קצב לב, לרוב טכיקרדיה סינוס.
- הפרעת הזעה [הזעת יתר מקומית (ידיים, רגליים, פנים) או כללית].
- הפרעות במערכת העיכול (עצירות, שלשולים, במקרים נדירים, חסימת מעיים).
- תפקוד לקוי של איברי האגן (בדרך כלל אצירת שתן) הוא נדיר ובדרך כלל קל וחולף.
- בתסמונת מילר-פישר, התמונה הקלינית נשלטת על ידי אטקסיה, שלרוב יש לה מאפיינים של המוח הקטן, במקרים נדירים - מעורב (רגיש למוח הקטן), ואופטלמופלגיה חלקית או מלאה, עצבי גולגולת אחרים עשויים להיפגע גם הם (VII, IX , איקס). פארזיס בדרך כלל קלה, ברבע מהמקרים יש הפרעות רגישות.
, , , ,
קריטריונים לאבחון לתסמונת גיליין-בארה
, , , , , , ,
סימנים של תסמונת גיליין-בארה נדרשים לאבחון
- א.חולשת שרירים מתקדמת ביותר מאיבר אחד
- ב. ארפלקסיה (היעדר רפלקסים בגידים)
מאפיינים של תסמונת גווילין-בארה התומכים באבחנה
- א. מאפיינים קליניים (רשומים לפי סדר חשיבות)
- התקדמות: חולשת שרירים מתפתחת במהירות אך מפסיקה להתקדם תוך 4 שבועות מההתחלה.
- סימטריה יחסית: סימטריה היא לעיתים רחוקות מוחלטת, אך אם איבר אחד מושפע, גם האיבר הנגדי מושפע (הערה: חולים מדווחים לרוב על תסמינים א-סימטריים בתחילת המחלה, אך עד לבדיקה הגופנית, הנגעים בדרך כלל סימטריים) .
- תסמינים סובייקטיביים ואובייקטיביים של הפרעה חושית.
- פגיעה בעצבי הגולגולת: paresis של שרירי הפנים.
- החלמה: מתחילה בדרך כלל 2-4 שבועות לאחר הפסקת התקדמות המחלה, אך לעיתים יכולה להתעכב למשך מספר חודשים. רוב החולים חווים התאוששות מלאה של התפקוד.
- הפרעות אוטונומיות: טכיקרדיה והפרעות קצב אחרות, יתר לחץ דם תנוחתי, יתר לחץ דם עורקי, הפרעות כלי דם.
- היעדר חום בתחילת המחלה (במקרים מסוימים, חום בתחילת המחלה אפשרי עקב מחלות ביניים או מסיבות אחרות; נוכחות חום אינה מוציאה מכלל את תסמונת גיליין-בארה, אך מגבירה את הסבירות להימצאות של מחלה אחרת, במיוחד פוליומיאליטיס).
- ב. אפשרויות
- הפרעות חושיות קשות עם כאב.
- התקדמות על פני 4 שבועות. לעיתים תיתכן התקדמות המחלה במשך שבועות רבים או נוכחות של הישנות קטנות.
- הפסקת ההתקדמות ללא התאוששות לאחר מכן או התמדה של תסמינים שיוריים מתמשכים חמורים.
- תפקודים של הסוגרים: בדרך כלל הסוגרים אינם נפגעים, אך במקרים מסוימים תיתכן הפרעות בשתן.
- מעורבות מערכת העצבים המרכזית: תסמונת Guillain-Barré משפיעה על מערכת העצבים ההיקפית, ואין עדות מהימנה לאפשרות של מעורבות של מערכת העצבים המרכזית. לחלק מהחולים יש אטקסיה מוחית גסה, סימני כף רגל חריגה מסוג extensor, dysarthria או רמה לא ברורה של פגיעה חושית (המרמזת על סוג מוליך של ליקוי), אך אלה אינם שוללים את האבחנה של תסמונת Guillain-Barré אם קיימים סימפטומים אופייניים אחרים. .
- ג. שינויים ב-CSF התומכים באבחון
- חלבון: שבוע לאחר הופעת המחלה, ריכוז החלבון בנוזל השדרה עולה (בשבוע הראשון הוא עשוי להיות תקין).
- ציטוזה: התוכן של לויקוציטים חד-גרעיניים בנוזל השדרה הוא עד 10 ל-1 μl (אם תכולת הלויקוציטים היא 20 ב-1 μl או יותר, יש צורך בבדיקה יסודית. אם תכולתם היא יותר מ-50 ב-1 μl, האבחנה של תסמונת Guillain-Barré נדחתה; היוצא מן הכלל הוא חולים עם זיהום HIV וליים בורליוזיס).
סימנים לתסמונת Guillain-Barré המעוררים ספקות לגבי האבחנה
- אסימטריה מתמשכת בולטת של פארזיס.
- הפרעות מתמשכות באגן.
- נוכחות של הפרעות באגן בתחילת המחלה.
- התוכן של לויקוציטים חד-גרעיניים בנוזל השדרה הוא יותר מ-50 ב-1 μl.
- נוכחות של לויקוציטים פולימורפונוקלאריים בנוזל השדרה.
- רמה ברורה של הפרעות תחושתיות
סימנים של תסמונת גילאן-בארה ששוללים את האבחנה
- שימוש לרעה נוכחי בממסים אורגניים נדיפים (שימוש לרעה בחומרים).
- הפרעות בחילוף החומרים של פורפירין, המרמזות על אבחנה של פורפיריה חריפה לסירוגין (הפרשה מוגברת של פורפובילינוגן או חומצה aminolevulinic בשתן).
- דיפטריה לאחרונה.
- נוכחות של תסמינים של נוירופתיה עקב שיכרון עופרת (פרזה של שרירי הגפה העליונה, לפעמים אסימטרית, עם חולשה חמורה של היד הפושטת) או עדות לשיכרון עופרת.
- נוכחות של לקויות חושיות בלבד.
- אבחון אמין של מחלה אחרת, המתבטאת בסימפטומים הדומים לתסמונת Guillain-Barré (פוליאומיאליטיס, בוטוליזם, פולינורופתיה רעילה).
טפסים
נכון לעכשיו, בתוך תסמונת Guillain-Barré, ישנם ארבע גרסאות קליניות עיקריות.
- פוליראדיקולונורופתיה דלקתית חריפה היא הצורה הקלאסית הנפוצה ביותר (85-90%) של תסמונת Guillain-Barré.
- צורות אקסונליות של תסמונת Guillain-Barré נצפות בתדירות נמוכה בהרבה (10-15%). נוירופתיה אקסונלית מוטורית חריפה מאופיינת בנגע מבודד של סיבים מוטוריים, הנפוץ ביותר באסיה (סין) ובדרום אמריקה. בנוירופתיה אקסונלית מוטורית-חושית חריפה, הן סיבים מוטוריים והן סיבים תחושתיים מושפעים, צורה זו קשורה למהלך ממושך ולפרוגנוזה לקויה.
- תסמונת מילר-פישר (לא יותר מ-3% מהמקרים) מאופיינת על ידי אופטלמופלגיה, אטקסיה מוחית וארפלקסיה עם פארזיס קלה בדרך כלל.
בנוסף לאלו העיקריים, לאחרונה הבחינו במספר צורות לא טיפוסיות נוספות של המחלה - פנדיסאוטונומיה חריפה, נוירופתיה חושית חריפה ופולינוירופתיה גולגולתית חריפה, הנצפות לעתים רחוקות מאוד.
, , , , , , ,
אבחון של תסמונת גילאן-בארה
בעת איסוף אנמנזה, יש להבהיר את ההיבטים הבאים.
- נוכחות של גורמים מזרזים. בכ-80% מהמקרים, התפתחות תסמונת Guillain-Barré קודמת למחלות או מצבים מסוימים תוך 1-3 שבועות.
- - זיהומים של מערכת העיכול, דרכי הנשימה העליונות או לוקליזציה אחרת. קשר עם זיהום מעיים הנגרם על ידי קמפילובקטר ג'יוני.לשורדים של קמפילובקטריוזיס יש סיכוי גבוה פי 100 לפתח תסמונת גווילין-בארה תוך חודשיים מהמחלה מאשר האוכלוסייה הכללית. תסמונת Guillain-Barré יכולה להתפתח גם לאחר זיהומים הנגרמים על ידי נגיפי הרפס (ציטומגלווירוס, וירוס אפשטיין-בר, אבעבועות רוח), Haemophilus influenzae,מיקופלזמה, חצבת, חזרת, ליים בורליוזיס וכו'. בנוסף, תסמונת Guillain-Barré יכולה להתפתח עם זיהום ב-HIV.
- חיסון (נגד כלבת, נגד טטנוס, נגד שפעת וכו').
- התערבויות כירורגיות או פציעות של כל לוקליזציה.
- נטילת תרופות מסוימות (תרופות טרומבוליטיות, איזוטרטינואין וכו') או מגע עם חומרים רעילים.
- לפעמים תסמונת Guillain-Barré מתפתחת על רקע מחלות אוטואימוניות (זאבת אדמנתית מערכתית) וגידולים (לימפוגרנולומטוזיס ולימפומות אחרות).
מחקר מעבדתי ואינסטרומנטלי
- מחקרים קליניים כלליים (ספירת דם כללית, בדיקת שתן כללית).
- בדיקת דם ביוכימית: ריכוז אלקטרוליטים בסרום, הרכב גזי דם עורקי. כאשר מתכננים טיפול ספציפי עם אימונוגלובולינים מסוג G, יש צורך לקבוע את שברי ה-Ig בדם. ריכוז נמוך של IgA קשור בדרך כלל למחסור התורשתי שלו, במקרים כאלה הסיכון לפתח הלם אנפילקטי גבוה (טיפול אימונוגלובולינים אסור).
- מחקרי CSF (ציטוזה, ריכוז חלבון).
- מחקרים סרולוגיים במקרה של חשד לתפקיד אטיולוגי של זיהומים מסוימים (סמנים של HIV, ציטומגלווירוס, וירוס אפשטיין-בר, Borrelia burgdorferi, Campylobacter jejuniוכו.). אם קיים חשד לפוליומיאליטיס, יש צורך במחקרים וירולוגיים וסרולוגיים (טיטר של נוגדנים בסרום מזווג).
- EMG, לתוצאותיו חשיבות מהותית לאישור האבחנה וקביעת צורת תסמונת Guillain-Barré. יש לקחת בחשבון שתוצאות EMG עשויות להיות תקינות במהלך השבוע הראשון של המחלה.
- שיטות הדמיית עצבים (MRI) אינן מאפשרות לאשר את האבחנה של תסמונת Guillain-Barré, אך עשויות להיות נחוצות לאבחנה מבדלת עם פתולוגיה של מערכת העצבים המרכזית (תאונה מוחית חריפה, דלקת מוח, מיאליטיס).
- ניטור תפקוד הנשימה החיצונית [קביעת היכולת החיונית של הריאות (VC) לזיהוי בזמן של אינדיקציות להעברת החולה לאוורור מכני.
- במקרים חמורים (במיוחד עם התקדמות מהירה של המחלה, הפרעות בולבריות, הפרעות אוטונומיות חמורות), כמו גם במהלך אוורור מכני, יש צורך לעקוב אחר האינדיקטורים החיוניים העיקריים (ביחידה לטיפול נמרץ): לחץ דם, א.ק.ג., דופק אוקסימטריה, תפקוד נשימתי ואחרים (בהתאם למצב הקליני הספציפי ולטיפול).
, , ,
קריטריונים נוירופיזיולוגיים לסיווג של תסמונת Guillain-Barré
תקין (כל הסימנים הבאים חייבים להיות נוכחים בכל העצבים הנבדקים)
- חביון מוטורי דיסטלי
- התמדה וחביון של גלי F
- CRV > 100% גבול תחתון של נורמלי.
- המשרעת של תגובת M במהלך גירוי בנקודה הדיסטלית היא > 100% מהגבול התחתון של נורמלי.
- משרעת תגובת ה-M במהלך גירוי בנקודה הפרוקסימלית היא > 100% מהגבול התחתון של נורמלי.
- היחס "משרעת תגובה M במהלך גירוי בנקודה הפרוקסימלית / משרעת תגובה M במהלך גירוי בנקודה הדיסטלית"> 0.5
נגע דמיילינציה ראשוני (דורש לפחות אחד מהסימנים בלפחות שני עצבים שנבדקו, או נוכחות של שני סימנים בעצב אחד אם כל שאר העצבים אינם מעוררים ומשרעת תגובת M בגירוי בנקודה הדיסטלית היא > 10% מהגבול התחתון של נורמלי).
- חביון מוטורי דיסטלי > 110% גבול עליון של נורמלי (> 120% אם המשרעת של תגובת M במהלך גירוי בנקודה הדיסטלית
- היחס "משרעת תגובה M במהלך גירוי בנקודה הפרוקסימלית / משרעת תגובה M במהלך גירוי בנקודה הדיסטלית" הוא 20% מהגבול התחתון של נורמה.
- חביון גלי F > 120% גבול עליון של נורמלי
נגע אקסונלי ראשוני
- היעדר כל הסימנים לעיל של דה-מיאלינציה בכל העצבים שנבדקו (נוכחות של אחד מהם באחד העצבים מקובלת אם משרעת תגובת M במהלך גירוי בנקודה הדיסטלית
עצבנות של עצבים
- לא ניתן לעורר את תגובת ה-M באף אחד מהעצבים בגירוי בנקודה הדיסטלית (או שניתן לעורר רק בעצב אחד עם המשרעת שלו
תבוסה לא בטוחה
אינו עומד בקריטריונים של אף אחד מהטפסים לעיל
צורה זו עשויה לכלול מקרים של אקסונופתיה חמורה ראשונית, דה-מיאלינציה דיסטלית חמורה עם חסימת הולכה, וניוון וולריאני משני לאחר דה-מיאלינציה; מבחינה נוירופיזיולוגית, אי אפשר להבחין ביניהם.
אינדיקציות להתייעצות עם מומחים אחרים
- הטיפול בחולים עם צורות חמורות של תסמונת Guillain-Barré מתבצע במשותף עם הרופא של היחידה לטיפול נמרץ.
- במקרה של הפרעות קרדיווסקולריות חמורות (יתר לחץ דם עורקי קשה מתמשך, הפרעות קצב), ייתכן שתידרש התייעצות עם קרדיולוג.
נתונים משיטות מחקר נוספות
אלקטרומיוגרפיה (EMG) היא בעלת ערך אבחנתי רב בתסמונת גיליין-בארה. וחקר מהירות הדחפים לאורך העצבים, כמו גם חקר נוזל מוחי. החל מהיום ה-3-7 לאחר הופעת התסמינים הראשונים, מחקר אלקטרו-פיזיולוגי מגלה האטה בהולכה לאורך המוטורית ו(במידה פחותה) לאורך סיבים תחושתיים, התארכות החביון הדיסטלי והתקופה הסמויה של גל ה-F, ירידה באמפליטודה של פוטנציאל הפעולה השריר הכולל (M-response ) ולעיתים פוטנציאל פעולה חושי, כמו גם בלוקים הולכה מוקדיים ואסימטריים, המעידים על פולינורופתיה דמיילינציה סגמנטלית. מאידך, בפולינוירופתיה אקסונלית מוטורית חריפה, משרעת פוטנציאל הפעולה התחושתי ומהירות ההולכה לאורך סיבי חושים עשויות להיות תקינות, אך ישנה ירידה במשרעת פוטנציאל הפעולה של השריר הכולל ורק האטה קלה בהולכה. לאורך סיבים מוטוריים. כאשר הן סיבים מוטוריים והן סיבים תחושתיים מושפעים, הן פוטנציאל הפעולה הכולל של השריר והן פוטנציאל הפעולה התחושתי יכולים להשתנות בצורה גסה, וקשה למדידה של חביון דיסטלי ומהירות הולכה, דבר המצביע על אקסונופתיה מוטורית חושית חמורה. בתסמונת מילר פישר, המתבטאת באטקסיה, אופתלמופלגיה וארעפלקסיה, כוח השריר נשאר ללא פגע, ומהירות ההולכה העצבית של EMG ועצבים עשויה להיות תקינה.
בעת מחקר נוזל מוחיבחולים עם תסמונת Guillain-Barré, מזוהה עלייה בתכולת החלבון לרמה העולה על 60 מ"ג/ד"ל עם ציטוזיס רגיל (לא יותר מ-5 תאים ב-1 μl). עם זאת, בימים הראשונים של המחלה, תכולת החלבון בנוזל השדרה עשויה להיות תקינה, בעוד שעלייה בציטוזיס ל-30 תאים ל-1 μl אינה שוללת את האבחנה של תסמונת Guillain-Barré.
מכיוון שביופסיה של עצב סוראל בדרך כלל אינה חושפת סימנים של דלקת או דה-מיילינציה, שיטה זו אינה נכללת במערך המחקרים הסטנדרטי ברוב החולים עם תסמונת Guillain-Barré, אך עשויה להיות חשובה במחקר מדעי. מחקרים פתולוגיים מצביעים על כך שבתסמונת Guillain-Barré, העצבים והשורשים הפרוקסימליים של עצבי עמוד השדרה מושפעים בעיקר: אצלם מתגלים בצקת, דה-מיילינציה מקטעית, חדירת האנדונאוריום על ידי תאים חד-גרעיניים, כולל מקרופאגים. תאים חד-גרעיניים מקיימים אינטראקציה גם עם תאי שוואן וגם עם מעטפת המיאלין. למרות שתסמונת Guillain-Barré היא פוליראדיקולונורופתיה, ניתן לזהות שינויים פתולוגיים גם במערכת העצבים המרכזית (CNS). ברוב 13 מקרי הנתיחה שלאחר המוות נמצאה הסתננות חד-גרעינית עם לימפוציטים ומקרופאגים פעילים בחוט השדרה, המדוללה אולונגאטה והפונס. עם זאת, דה-מיילינציה ראשונית לא זוהתה ב-CNS. במהלך הארוך, הסוג השולט של תאי דלקת במערכת העצבים המרכזית והפריפריאלית הופעלו מקרופאגים, בנוסף התגלו שם לימפוציטים CD4+ ו-CD8+.
, , , , , , , , , , , ,
אבחון דיפרנציאלי
יש להבדיל בין תסמונת Guillain-Barré ממחלות אחרות המתבטאות בפארזיס פריפריאלי חריף, בעיקר מפוליומיאליטיס (במיוחד בילדים צעירים) ופולינוירופתיות אחרות (דיפתריה, עם פורפיריה). בנוסף, נגעים של חוט השדרה וגזע המוח (מיאליטיס רוחבי, שבץ במערכת הוורטברובזילרית) ומחלות עם פגיעה בהעברה עצבית-שרירית (myasthenia gravis, בוטוליזם) יכולים לקבל תמונה קלינית דומה.
- באבחון מבדל של פוליומיאליטיס יש לקחת בחשבון את נתוני ההיסטוריה האפידמיולוגית, נוכחות חום בתחילת המחלה, תסמינים ממערכת העיכול, אסימטריה של הנגע, היעדר הפרעות רגישות אובייקטיביות וציטוזה גבוהה. בנוזל השדרה. האבחנה של פוליומיאליטיס מאושרת על ידי בדיקה וירולוגית או סרולוגית.
- פולינוירופתיה בפורפיריה חריפה לסירוגין עשויה להידמות לתסמונת Guillain-Barré, אך, ככלל, היא מלווה במגוון תסמינים פסיכופתולוגיים (הזיות, הזיות וכו') וכאבי בטן עזים. האבחנה מאושרת על ידי זיהוי ריכוז מוגבר של פורפובילינוגן בשתן.
- מיאליטיס רוחבי מאופיינת בתפקוד מוקדם ומתמשך של איברי האגן, נוכחות של רמה של הפרעות תחושתיות והיעדר נזק לעצבי הגולגולת.
- תסמינים, המזכירים את אלה בתסמונת Guillain-Barré, אפשריים עם אוטמים נרחבים של גזע המוח עם התפתחות של טטרפרזיס, אשר בתקופה החריפה יש מאפיינים היקפיים. עם זאת, מקרים כאלה מתאפיינים בהתפתחות חריפה (בדרך כלל תוך דקות ספורות) וברוב המקרים דיכאון תודעה (תרדמת), שאינו נצפה בתסמונת Guillain-Barré. האבחנה הסופית מאושרת על ידי MRI.
- מיאסטניה גרביס שונה מתסמונת Guillain-Barré בשונות הסימפטומים, היעדר הפרעות תחושתיות ושינויים אופייניים ברפלקסים בגידים. האבחנה מאושרת על ידי EMG (גילוי תופעת ירידה) ובדיקות פרמקולוגיות.
- בוטוליזם, בנוסף לנתונים האפידמיולוגיים הרלוונטיים, מאופיין בסוג יורד של התפשטות פארזיס, שימור רפלקסים בגידים בחלק מהמקרים, היעדר הפרעות תחושתיות ושינויים בנוזל השדרה.
טיפול בתסמונת Guillain-Barré
מטרות הטיפול בתסמונת Guillain-Barré הן שמירה על תפקודים חיוניים, עצירת התהליך האוטואימוני בעזרת טיפול ספציפי ומניעת סיבוכים.
אינדיקציות לאשפוז
כל החולים בתסמונת גיליין-בארה נתונים לאשפוז בבית חולים עם יחידה לטיפול נמרץ ויחידה לטיפול נמרץ.
טיפולים לא תרופתיים לתסמונת גיליין-בארה
כ-30% מהמקרים של תסמונת Guillain-Barré מפתחים כשל נשימתי חמור (עקב פארזיס של הסרעפת ושרירי הנשימה), המחייב אוורור מכני. אינדיקציות לאינטובציה עם אוורור מכני נוסף - ירידה ב-VC ל-15-20 מ"ל/ק"ג, P a O 2 50 מ"מ כספית. משך האוורור המכני (ממספר ימים עד חודשים) נקבע על בסיס אישי, תוך התמקדות ביכולת החיונית, בשיקום רפלקס הבליעה והשיעול ובדינמיקה הכללית של המחלה. נתק את המטופל ממכשיר ההנשמה בהדרגה, דרך השלב של אוורור מאולץ לסירוגין.
במקרים חמורים עם paresis חמור, טיפול נאות הוא בעל חשיבות בסיסית למניעת סיבוכים הקשורים לחוסר תנועה ממושך של המטופל (פצעי שינה, זיהומים, סיבוכים טרומבואמבוליים וכו'): שינוי תקופתי (כל שעתיים או יותר) של תנוחת המטופל, טיפול בעור , מניעת שאיפה [השכלה של חלל הפה והאף, הזנה דרך צינור האף, תברואה של קנה הנשימה והסימפונות (בזמן אוורור מכני)], שליטה בתפקודי שלפוחית השתן והמעיים, התעמלות פסיבית ועיסוי הגפיים וכו'. .
עם ברדיאריתמיה מתמשכת עם איום של אסיסטולה, ייתכן שיהיה צורך להתקין קוצב לב זמני.
טיפול תרופתי ופלזפרזה
כטיפול ספציפי לתסמונת Guillain-Barré, שמטרתו לעצור את התהליך האוטואימוני, נעשה כיום שימוש בטיפול דופק עם אימונוגלובולינים מסוג G ופלזמפרזיס. שיטות טיפול ספציפיות מיועדות למהלך חמור (על פי סולם חומרת הליקוי המוטורי בצפון אמריקה 4 ו-5 נקודות) ובינוני (2-3 נקודות) של המחלה. האפקטיביות של שתי השיטות זהה בערך, היישום בו-זמני אינו מעשי. שיטת הטיפול נבחרת על בסיס אישי, תוך התחשבות בזמינות, התוויות נגד אפשריות וכו'.
- פלסמפרזיס הוא טיפול יעיל לתסמונת Guillain-Barré, המפחית באופן משמעותי את חומרת הפרזיס, את משך האוורור המכני ומשפר את התוצאה התפקודית. בדרך כלל מבוצעות 4-6 פעולות במרווח של יום אחד; נפח הפלזמה שיש להחליף בפעולה אחת חייב להיות לפחות 40 מ"ל/ק"ג. כמדיה חלופית משתמשים בתמיסת נתרן כלוריד 0.9%, ריאופוליגליוקין ותמיסת אלבומין. פלזמפרזיס היא התווית יחסית לאי ספיקת כבד, פתולוגיה חמורה של מערכת הלב וכלי הדם, הפרעות בקרישת הדם ונוכחות של זיהומים. סיבוכים אפשריים הם הפרעות המודינמיות (ירידה בלחץ הדם), תגובות אלרגיות, הפרעות אלקטרוליטים, הפרעות דימומיות, התפתחות המוליזה. כולם נדירים למדי.
- אימונוגלובולינים מסוג G ניתנים לווריד במינון של 0.4 גרם/ק"ג פעם ביום למשך 5 ימים. טיפול באימונוגלובולין, כמו פלזמהפרזה, מקצר את משך השהייה באוורור מכני ומשפר את התוצאה התפקודית. תופעות הלוואי השכיחות ביותר הן כאבי ראש וכאבי שרירים, חום, בחילות; ניתן להפחית את חומרתן על ידי הפחתת קצב העירוי. תופעות לוואי חמורות, כגון תרומבואמבוליזם, דלקת קרום המוח אספטית, המוליזה, אי ספיקת כליות חריפה ועוד, הן נדירות ביותר. אימונוגלובולין אנושי תקין הוא התווית נגד במחסור מולד ב-IgA ובהיסטוריה של תגובות אנפילקטיות לתכשירי אימונוגלובולינים.
טיפול סימפטומטי בתסמונת Guillain-Barré
- טיפול עירוי לתיקון הפרות של איזון חומצה-בסיס, מים-אלקטרוליטים, יתר לחץ דם עורקי חמור.
- עם יתר לחץ דם עורקי חמור מתמשך, נקבעות תרופות להורדת לחץ דם (חוסמי בטא או חוסמי תעלות סידן איטיות).
- עם טכיקרדיה חמורה, חוסמי בטא (פרופרנולול) נקבעים, עם ברדיקרדיה - אטרופין.
- עם התפתחות של זיהומים ביניים, יש צורך בטיפול אנטיביוטי (משתמשים בתרופות רחבות טווח, כגון פלואורוקינולונים).
- למניעת פקקת ורידים עמוקים ותסחיף ריאתי, הפרין במשקל מולקולרי נמוך נקבע במינונים מניעתיים פעמיים ביום).
- לכאבים ממקור נוציספטיבי (שרירי, מכני), מומלץ אקמול או NSAID, במקרה של כאב נוירופתי, התרופות הנבחרות הן gabapentin, carbamazepine, pregabalin.
טיפול כירורגי בתסמונת Guillain-Barré
אם יש צורך באוורור מכני לטווח ארוך (יותר מ-7-10 ימים), רצוי לבצע טרכאוסטומיה. בהפרעות בולבריות קשות וממושכות, עשויה להידרש גסטרוסטומיה.
עקרונות כלליים לטיפול בתסמונת Guillain-Barré
טיפול בביטויים המתפתחים בצורה חריפה ומתגברת במהירות של תסמונת Guillain-Barré מצריך טיפול תומך ביחידה לטיפול נמרץ, כמו גם חשיפה למנגנוני החיסון של המחלה. חולים עם תסמונת Guillain-Barré צריכים להתאשפז לצורך מעקב קפדני אחר תפקודים נשימתיים ואוטונומיים. ככל שהשיתוק מצטבר מהר יותר, כך גדל הסיכוי שיידרש אוורור מכני. בתקופה של התגברות הסימפטומים, יש צורך בבדיקה נוירולוגית קבועה, הערכת קיבולת הריאות, שמירה על סבלנות דרכי הנשימה עם שאיבה סדירה של ריר. בשלב מוקדם של המחלה, יש צורך בדריכות מתמדת, שכן גם בהיעדר הפרות ברורות של תפקודי הנשימה והבולבר, שאיפה קטנה יכולה להגביר באופן משמעותי את התפקוד האוטונומי ולעורר אי ספיקת נשימה.
השיפור בפרוגנוזה והפחתה בתמותה בתסמונת גיליין-בארה שהושג בשנים האחרונות נובע בעיקר מהאשפוז מוקדם של חולים ליחידות טיפול נמרץ. אינדיקציות להעברת המטופל ליחידה לטיפול נמרץ ובחינת נושא האינטובציה עשויות להיות ירידה ביכולת הריאות מתחת ל-20 מ"ל/ק"ג וקושי בהוצאת הפרשות מדרכי הנשימה. מטרת ההעברה המוקדמת היא למנוע אינטובציה חירום במצב של אי ספיקת נשימה חמורה עם תנודות דרמטיות בלחץ הדם ובקצב הלב שעלולות לגרום לתפקוד לקוי או לאוטם שריר הלב. אחת המשימות החשובות ביותר של טיפול תחזוקה היא מניעה וטיפול בזמן של דלקות ריאות ודרכי השתן, כמו גם מניעת פקקת ורידים עמוקים של הרגל ותסחיף ריאתי לאחר מכן על ידי מתן תת עורי של הפרין (5000 IU 2 פעמים ביום) . כמו כן, יש צורך לעקוב אחר התזונה ותפקוד המעיים. מכיוון שלפרעה אוטונומית יש השפעה משמעותית על התמותה, יש צורך במעקב מתמיד אחר פעילות הלב ולחץ הדם.
אחד ההיבטים החשובים בסיוע למטופלים עם תסמונת גווילין-בארה ביחידה לטיפול נמרץ, אשר עם זאת, לא תמיד נלקח בחשבון, הוא תיקון של חרדה קשה, העלולה להיגרם על ידי קיבוע מוחלט של החולה על רקע של אינטליגנציה שלמה. בהקשר זה, תמיכה פסיכולוגית חשובה. החולים צריכים להסביר את מהות המחלה, את תכונות מהלך שלה, כולל אפשרות התקדמות, כדי להכיר את שיטות הטיפול בשלבים שונים. חשוב להם להסביר שהסבירות להחלמה מלאה גבוהה מאוד, גם אם הם יהיו באוורור מכני זמן מה. יצירת מגע בעזרת תנועות עיניים מפחיתה את תחושת הבידוד של המטופל מהעולם. מניסיוננו, מתן 0.5 מ"ג לוראזפאם כל 4-6 שעות יעיל להזיות ליליות. כמו כן, ניתן לרשום 0.5 מ"ג ריספרידון או 0.25 מ"ג אולנזפין.
הפרקטיקה של טיפול בתסמונת גיליין-בארה עברה שינויים משמעותיים במהלך העשור האחרון. לדוגמה, היעילות של פלזמפרזיס הוכחה. למרות שמנגנון הפעולה שלו לא ידוע, מאמינים שהוא עשוי להיות קשור להפרשת נוגדנים, ציטוקינים, משלים ומתווכים אחרים של התגובה הדלקתית החיסונית. מחקר פתוח, רב-מרכזי בצפון אמריקה, שהשווה תוצאות בין פלזמפרזיס ללא טיפול ספציפי הראה שחמישה ימים רצופים של פלזמפרזיס הפחיתו את האשפוז והביאו לשיפור גדול יותר מאשר בביקורת. הטיפול היה יעיל יותר אם התחיל בשבוע הראשון של המחלה. תוצאות דומות התקבלו על ידי הקבוצה הקואופרטיבית הצרפתית, אשר ערכה מחקר רב-מרכזי אקראי והראתה כי ארבעה מפגשים של פלזמהזיס מובילים להחלמה מהירה יותר ב-220 חולים שנכללו במחקר (French Cooperative Group, 1987). מחקר שנערך באותם חולים לאחר שנה הראה ששיקום מלא של כוח השריר צוין ב-71% מהחולים שעברו פלזמפרזיס, ורק ב-52% מהחולים בקבוצת הביקורת (French Cooperative Group, 1992). המחקר הבא השווה את היעילות של מספרים שונים של פגישות פלזמהזיס ב-556 חולים עם תסמונת Guillain-Barré עם חומרת סימפטומים משתנה (French Cooperative Group, 1997). בחולים עם תסמינים קלים שעברו שני מפגשים של פלזמפרזיס, ההחלמה הייתה משמעותית יותר מאשר בחולים שמשטר הטיפול שלהם לא כלל פלזמפרזיס. בחולים סימפטומטיים בינוניים, ארבעה מפגשי פלזמהזיס היו יעילים יותר משני מפגשי פלזמהרזיס. יחד עם זאת, שישה מפגשים של פלזמפרזיס לא עלו על ארבעה מפגשים מבחינת יעילות בחולים עם תסמינים בינוניים וחמורים כאחד. נכון לעכשיו, רוב המרכזים המתמחים בטיפול בתסמונת גיליין-בארה עדיין משתמשים בחמישה עד שישה מפגשים, המתבצעים על פני 8-10 ימים, כדי להימנע מהלחץ הכרוך בהליך היומיומי. עירוי החלפה מתבצע באמצעות צנתר שילי. פלזמפרזיס יעילה גם בילדים עם תסמונת גיליין-בארה, ומאיצה את תהליך החזרת היכולת לנוע באופן עצמאי. למרות שפלזפרזה היא פרוצדורה בטוחה יחסית, השימוש בה בתסמונת Guillain-Barré מצריך טיפול מיוחד בשל הסיכון להפרעות בתפקוד אוטונומי בחולים ונטייתם לפתח זיהומים.
מתן תוך ורידי של מינונים גבוהים של אימונוגלובולין מוכר גם כטיפול יעיל לתסמונת Guillain-Barré, שיכול להפחית משמעותית את משך המחלה וחומרתה. כמו במקרה של פלזמפרזיס, מנגנון הפעולה הטיפולית של אימונוגלובולין נותר לא ברור. מוצע כי הוא יכול לחסל נוגדנים פתוגניים עקב נוגדנים אנטי-אידיוטיפיים, לחסום את רכיב ה-Fc של נוגדנים על תאי מטרה, וגם לעכב שקיעת משלימים, להמיס קומפלקסים חיסוניים, להחליש את תפקודי הלימפוציטים, לשבש את הייצור או להפריע ליישום הציטוקינים. פונקציות. אימונוגלובולין נקבע במינון כולל של 2 גרם / ק"ג, הניתן על פני 2-5 ימים. בניסוי אקראי שהשווה את ההשפעה של אימונוגלובולין ופלזמפרזיס, הוכח כי עם פלזמפרזיס חל שיפור בממוצע לאחר 41 יום, ובאימונוגלובולין לאחר 27 ימים. בנוסף, לחולים שקיבלו אימונוגלובולין היו פחות סיבוכים באופן משמעותי ונזקקו לאוורור מכני במידה פחותה. זקנה הייתה הגורם הפרוגנוסטי השלילי העיקרי. מחקר רב-מרכזי אקראי שלאחר מכן של פלזמהרזיס ואימונוגלובולין ב-383 חולים שקיבלו מרשם לשיטות אלו במהלך השבועיים הראשונים לאחר הופעת התסמינים הראה שלשתי השיטות יעילות דומה, אך לשילוב שלהן אין יתרונות משמעותיים על פני שימוש בכל אחת מהשיטות בנפרד. .
החדרת אימונוגלובולין במינון של 2 גרם/ק"ג למשך יומיים הוכיחה את עצמה כשיטה יעילה ובטוחה לטיפול בילדים עם תסמונת Guillain-Barré חמורה. תופעות הלוואי היו קלות ונצפו לעתים רחוקות. חלק מהחולים, במיוחד אלו שסבלו ממיגרנה, סבלו מכאב ראש, שלעיתים מלווה בדלקת קרום המוח אספטית עם פלוציטוזיס בנוזל השדרה. לעיתים נצפו גם צמרמורות, חום ומיאלגיה, כמו גם הפרעה חריפה בתפקוד כלייתי עם התפתחות אי ספיקת כליות. עם כניסת האימונוגלובולין מתאפשרת תגובה אנפילקטית, במיוחד אצל אנשים עם מחסור באימונוגלובולין A. החיסרון העיקרי של אימונוגלובולין ושל פלזמהפרזה כאחד הוא העלות הגבוהה. עם זאת, ברור שיעילותם של טיפולים אלו גוברת על כך, שניכרת גם בעידן עשיית הכסף הזה.
במחקר כפול-סמיות, מבוקר פלצבו, רב-מרכזי ב-242 חולים עם תסמונת Guillain-Barré, קורטיקוסטרואידים תוך ורידי במינון גבוה (methylprednisolone, 500 מ"ג ביום למשך 5 ימים) לא השפיעו על אף אחד ממדדי התוצאה של תסמונת Guillain-Barré. בר, כמו גם הסבירות להישנותו. במחקר פתוח שלאחר מכן, שבו טופלו 25 חולים עם תסמונת Guillain-Barré באימונוגלובולין IV (0.4 גרם/ק"ג/יום למשך 5 ימים) ומתילפרדניזולון (500 מ"ג ליום למשך 5 ימים), הושווה ההשפעה לנתוני הביקורת שהתקבלו. מוקדם יותר עם שימוש באימונוגלובולין אחד. בשילוב של אימונוגלובולין ומתילפרדניזולון, ההחלמה הייתה טובה יותר, בעוד שב-76% מהחולים עד סוף השבוע הרביעי חל שיפור בשלב תפקודי אחד לפחות - בקבוצת הביקורת נרשמה דרגת התאוששות דומה רק ב- 53% מהחולים. זה עשוי להצביע על כך שקורטיקוסטרואידים עדיין עשויים למלא תפקיד בטיפול בתסמונת Guillain-Barré. יש צורך בניסויים קליניים אקראיים כדי להבהיר נושא זה ולקבוע האם יש שיפור משמעותי בתוצאה כאשר מוסיפים קורטיקוסטרואידים תוך ורידי לפלזמפרזיס או אימונוגלובולין.
ניהול נוסף
לאחר תום התקופה החריפה, יש צורך בצעדי שיקום מורכבים, שתוכניתם נערכת על בסיס אינדיבידואלי, בהתאם לחומרת הסימפטומים השיוריים (תרפיה בפעילות גופנית, עיסוי וכו', בעוד הליכים תרמיים הם התווית נגד!).
יש ליידע חולים עם תסמונת Guillain-Barré על הצורך להקפיד על משטר הגנה לפחות 6-12 חודשים לאחר סיום המחלה. עומס יתר פיזי, התחממות יתר, היפותרמיה, בידוד מופרז, צריכת אלכוהול אינם מקובלים. גם בתקופה זו יש להימנע מחיסונים.
תַחֲזִית
התמותה בתסמונת Guillain-Barré עומדת על 5% בממוצע. סיבת המוות עשויה להיות כשל נשימתי, מוות אפשרי גם עקב דלקת ריאות בשאיפה, אלח דם וזיהומים נוספים, תסחיף ריאתי. התמותה עולה משמעותית עם הגיל: בילדים מתחת לגיל 15 היא אינה עולה על 0.7%, בעוד שבאנשים מעל גיל 65 היא מגיעה ל-8.6%. גורמים פרוגנוסטיים שליליים אחרים להחלמה מלאה כוללים תקופה ארוכה (יותר מחודש) של אוורור מכני, נוכחות של מחלות ריאה קודמות.
רוב החולים (85%) חווים החלמה תפקודית מלאה תוך 6-12 חודשים. תסמינים שיוריים מתמשכים נמשכים בכ-7-15% מהמקרים. מנבאים של תוצאה תפקודית לא חיובית הם גיל מעל 60 שנים, מהלך מתקדם במהירות של המחלה ומשרעת נמוכה של תגובת M בעת גירוי בנקודה הדיסטלית (מרמזת על נזק חמור לאקסונים). שיעור ההישנות של תסמונת גיליין-בארה הוא כ-3-5%.
