RCHD (Републикански център за развитие на здравеопазването на Министерството на здравеопазването на Република Казахстан)
Версия: Клинични протоколи на Министерството на здравеопазването на Република Казахстан - 2016 г
Синдром на Гилен-Баре (G61.0)
Неврология
Главна информация
Кратко описание
Одобрено
Съвместна комисия по качеството на медицинските услуги
Министерство на здравеопазването и социалното развитие на Република Казахстан
от 29 ноември 2016 г
Протокол No16
Синдром на Guillain-Barré(Синдром на Guillain-Barrés) (GBS) е остра, бързо прогресираща автоимунна лезия на периферната нервна система, проявяваща се под формата на парестезия на крайниците, мускулна слабост и/или вяла парализа (монофазна имуномедиирана невропатия).
Синоними на синдрома на Guillain-Barré: остра възпалителна демиелинизираща полиневропатия, остра идиопатична полиневропатия, инфекциозен полиневрит (полиневропатия), остър полирадикулит, синдром на Guillain-Barré-Strohls, синдром на Landry-Guillain-Barrés, синдром на Landry-Guillain-Barré-Strohls синдром, възходяща парализа на Ландри (Landry'sascendingparalysis), френски полиомиелит (Frenchpolio) и др.
Характеристика на това заболяване е самоограничаващ се, монофазен курс с изключително редки рецидиви.
Корелация между кодовете по МКБ-10 и МКБ-9
| КодMKB-10 | Код по ICD-9 | ||
|
G61.0 |
Синдром на Guillain-Barré |
357.0 |
Синдром на Guillain-Barré |
Дата на разработване/ревизиране на протокола: 2016 г
Потребители на протокола: ОПЛ, терапевти, реаниматори, невропатолози (възрастни, деца).
Скала на нивото на доказателства:
| НО | Висококачествен мета-анализ, систематичен преглед на RCT или големи RCT с много ниска вероятност (++) за отклонение, чиито резултати могат да бъдат обобщени за подходяща популация. |
| AT | Висококачествен (++) систематичен преглед на кохортни или случай-контролни проучвания или висококачествени (++) кохортни или случай-контролни проучвания с много нисък риск от пристрастия или RCT с невисок (+) риск от пристрастия, резултатите от които може да се разшири до съответната популация. |
| ОТ |
Кохорта или случай-контрола или контролирано изпитване без рандомизация с нисък риск от отклонение (+). Резултати, които могат да бъдат обобщени за подходяща популация или RCTs с много нисък или нисък риск от отклонение (++ или +), които не могат да бъдат директно обобщени за подходяща популация. |
| д | Описание на поредица от случаи или неконтролирано проучване или експертно мнение. |
Класификация
Класификация
GBS се класифицира както като невроинфекция, така и като състояние след инфекция. Има няколко форми на GBS, които се различават по хода на патологичния процес, първичната точка на приложение на автоимунната агресия (нервна обвивка или аксонален прът), прогнозата за възстановяване и клиничните прояви.
Според съвременните концепции има най-малко 8 разновидности (клинични варианти / подтипове) на синдрома на Гилен-Баре:
1) остра възпалителна демиелинизираща полиневропатия (класическа форма на синдром на Guillain-Barré);
2) остра моторно-сензорна аксонална невропатия (AMSAN);
3) остра моторно-аксонална невропатия (ОМАН);
4) Синдром на Милър-Фишър (MFS);
5) остра паавтономна невропатия (остър паавтономен синдром на Guillain-Barré, остра пандизавтономия);
6) стволов енцефалит Bickerstaff (Bickerstaff);
7) фаринго-цервико-брахиален вариант;
8) остра черепна полиневропатия.
Съществуват и опции за комбиниране на синдрома на Милър-Фишер с други форми на синдрома на Гилен-Баре (синдром на припокриване на MFS/GBS).
GBS също се класифицира според тежестта на състоянието в зависимост от клиничните прояви:
Леката форма се характеризира с липса или минимална пареза, която не причинява значителни затруднения при ходене и самообслужване;
При умерена тежест има нарушение на ходенето, ограничаване на движението на пациента или изискване на външна помощ или подкрепа;
при тежка форма на заболяването пациентът е прикован на легло и се нуждае от постоянна грижа, често се наблюдава дисфагия;
При изключително тежка форма пациентите се нуждаят от изкуствена вентилация на белите дробове (АЛВ) поради слабост на дихателната мускулатура.
Неврофизиологични критерии за класифициране на GBS (Р.
Хадън,
д.
Корнблат,
Р.
Хюгесетал., 1998).
Група с първична демиелинизираща лезия:
наличието на поне един от следните признаци в поне 2 нерва или два признака в един нерв е необходимо, ако всички останали нерви са невъзбудими и амплитудата на М-отговора в дисталната точка е 10% или повече от долна граница на нормата:
Скорост на разпространение на възбуждане (ERV) по-малко от 90% от долната граница на нормата или по-малко от 85% с амплитудата на М-отговора в дисталната точка по-малка от 50% от долната граница на нормата;
Дисталната латентност на М-отговора надвишава горната граница на нормата с повече от 10% или с повече от 20%, ако амплитудата на М-отговора в дисталната точка е под долната граница на нормата;
наличие на блок на дисперсия или възбуждане;
Латентността на F-вълната надвишава горната граница на нормата с повече от 20%.
Група с първична аксонална лезия:
няма признаци на демиелинизация, изброени по-горе, в който и да е нерв (с изключение на всеки един признак в 1 нерв, ако амплитудата на М-отговора в дисталната точка е повече от 10% под долната граница на нормата) и най-малко в два нерва амплитудата на М-отговора в дисталната точка е повече от 80% под долната граница на нормата.
Група с невъзбудими нерви:
· М-отговорът не може да бъде регистриран в нито един от изследваните нерви или е наличен само в един нерв с амплитуда в дисталната точка над 10% под долната граница на нормата.
Неопределена група:
· Промените, открити по време на стимулация ENMG, не отговарят на критериите на нито една от горните групи.
Диагностика (амбулатория)
ДИАГНОСТИКА НА АМБУЛАТОРНО НИВО
Диагностични критерии:
Оплаквания:
При нарастваща мускулна слабост в ръцете и/или краката;
изтръпване и намалена чувствителност;
Повишена чувствителност (тактилна, температурна и др.) в ръцете и краката;
болка в гърба, рамото и тазовия пояс;
Затруднено преглъщане както на твърди храни, така и на течности;
нарушение на дихателните функции, до липсата на самостоятелно дишане, поради отслабване на дихателните мускули, отслабване на гласа и кашлица;
нарушение на сърдечната честота, при някои може да бъде много ускорена, при други забавена;
Парализа на лицевите мускули
Повишено изпотяване
колебания в кръвното налягане
възможна поява на неконтролирано отделяне на урина;
Загуба на сухожилни рефлекси
нестабилна и нестабилна походка, нарушена координация на движенията;
промени в обема на корема, това се случва, защото за човек е трудно да диша с помощта на диафрагмата и той е принуден да използва коремната кухина;
Намалена зрителна острота - най-често се наблюдават бифуркация и страбизъм.
Симптомите са присъщи както на възрастни, така и на деца и новородени.
Анамнеза: GBS се развива, като правило, 1-3 седмици след инфекциозно заболяване (ТОРС, грип, синузит, бронхит, пневмония, тонзилит, морбили, паротит, диария и др.).
Неврологичните симптоми се появяват внезапно; повечето пациенти имат болка и парестезия.
При снемане на анамнеза е важно да се изяснят следните аспекти.
Наличие на провокиращи фактори. В приблизително 80% от случаите развитието на синдрома на Guillain-Barré се предшества от определени заболявания или състояния в рамките на 1-3 седмици.
Инфекции на стомашно-чревния тракт, горните дихателни пътища, могат да се развият след чревна инфекция, причинена от Campylobacterjejuni, след инфекции, причинени от херпесни вируси (цитомегаловирус, Epstein-Barr вирус, варицела-зостер вирус), Haemophilus influenzae, микоплазми, морбили, паротит, лаймска инфекция. борелиоза и др. В допълнение, при HIV инфекция е възможно развитието на синдром на Guillain-Barré.
Ваксинация (против бяс, против тетанус, срещу грип и др.);
хирургични интервенции или наранявания от всякаква локализация;
приемане на определени лекарства (тромботични лекарства, изотретиноин и др.) или контакт с токсични вещества;
Понякога синдромът на Guillain-Barré се развива на фона на автоимунни (системен лупус еритематозус) и туморни (лимфогрануломатоза и други лимфоми) заболявания.
Има определен модел в увеличаването на симптомите, въз основа на който се разграничават 3 етапа на заболяването:
прогресия (1-4 седмици) - появата и засилването на неврологични разстройства;
плато (10-14 дни) - стабилизиране на клиничната картина;
Обратно развитие (от няколко седмици до 2 години) - възстановяване на нормалното функциониране на тялото.
Физическо изследваневключва:
· общ соматичен статус: общо състояние и неговата тежест, телесна температура, измерване на теглото на пациента, преглед на кожата, дишане, пулс, кръвно налягане, състояние на вътрешните органи (бели дробове, сърце, черен дроб, бъбреци и др.).
· неврологичен статус:
Неврологичният преглед е насочен към идентифициране и оценка на тежестта на основните симптоми на синдрома на Guillain-Barré - сензорни, двигателни и вегетативни нарушения.
оценка на силата на мускулите на крайниците;
Изследване на рефлексите - за синдрома на Guillain-Barré е характерна арефлексията (т.е. липсата на повечето рефлекси);
оценка на чувствителността - наличие на кожни участъци с усещане за изтръпване или изтръпване;
оценка на функцията на тазовите органи - евентуално краткотрайна уринарна инконтиненция;
Оценка на функцията на малкия мозък - наличие на нестабилност в позицията на Ромберг (стоене с протегнати пред себе си ръце и затворени очи), некоординирани движения;
Оценка на движенията на очните ябълки - при синдрома на Guillain-Barré е възможна пълна липса на способността за движение на очите;
Провеждане на вегетативни тестове - за оценка на увреждането на нервите, които инервират сърцето;
Оценява се реакцията на сърцето към рязко издигане от легнало положение, физическа активност;
Оценка на функцията за преглъщане.
Оценката на тежестта на двигателния дефицит при деца на възраст над 3 години се извършва по северноамериканската скала:
Етап 0 синдром на Guillain-Barré е норма;
1 етап - минимални двигателни нарушения;
Етап II - способността да се изминат 5 м без опора или опора;
Етап III - способността да се изминат 5 м с опора или опора;
Етап IV - невъзможност за изминаване на 5 м с опора или опора (прикован към легло или инвалидна количка);
Етап V на синдрома на Guillain-Barre - необходимостта от изкуствена вентилация на белите дробове;
Етап VI - смърт.
В клиничната практика за оценка на тежестта на двигателните нарушения се използва скалата за сила на мускулите на крайниците (A. Szobor, 1976).
0 точки - няма движения в мускула.
1 точка - минимални движения в мускула, но пациентът не задържа тежестта на крайника.
2 точки - пациентът държи тежестта на крайника, но съпротивлението на изследователя е минимално.
3 точки - пациентът се съпротивлява на усилията за промяна на позицията на крайника, но е незначително.
4 точки - пациентът се съпротивлява добре на усилията за промяна на позицията на крайника, но има известно намаляване на силата.
5 точки - мускулната сила съответства на възрастта и конституционната норма на субекта.
Клинични варианти на AIDP
| опция | Основни клинични симптоми |
| с типична клинична картина | |
| Остра възпалителна демиелинизираща полирадикулоневропатия (типичен GBS вариант) (>85%) | Слабост в крайниците със сравнително леки сензорни нарушения (възможно изолирани двигателни нарушения). |
| Остра моторна аксонална полиневропатия (>5%) | Слабост в крайниците без промяна в усещането. Дълбоките рефлекси могат да бъдат запазени. Бързо възстановяване на функциите. Най-често се среща при деца. |
| Остра моторно-сензорна аксонална полиневропатия (>1%) | Слабост и сензорни нарушения в крайниците. Бързо развитие на тежък двигателен дефицит с бавно и непълно възстановяване. Най-често се среща при възрастни. |
| С нетипична клинична картина | |
| Синдром на Милър-Фишър (>3%) | Комбинация от атаксия, предимно от малкомозъчен тип, с арефлексия, офталмополегия и понякога лека слабост в крайниците. Чувствителността обикновено е запазена. |
Лабораторни изследвания:
KLA - за изключване на възпалително заболяване на вътрешните органи, придружено от полиневропатичен синдром;
кръвен тест за захар (за изключване на диабетна полиневропатия);
биохимични кръвни изследвания - креатин, урея, AST, ALT, билирубин (за изключване на метаболитна полиневропатия);
· кръвен тест за газовия състав, за концентрацията на електролити - биохимичните кръвни изследвания помагат да се изключат метаболитни полиневропатии;
PCR кръв за вируси на хепатит - за изключване на полиневропатичен синдром при хепатит
кръвен тест за HIV инфекция - за изключване на полиневропатия, свързана с HIV инфекция;
· PCR кръвен тест за вирусни инфекции (цитомегаловирус, Epstein-Barr virus, Borreliaburgdorferi, Campylobacterjejuni и др.) - при съмнение за инфекциозна етиология на GBS.
Инструментални изследвания:
Рентгенография на гръдни органи - за изключване на възпалителни белодробни заболявания или свързани белодробни усложнения с отслабване на дихателната мускулатура;
ЕКГ - за откриване или изключване на вегетативни сърдечни аритмии в клиниката на GBS;
Ултразвук на коремни органи - заболяванията на вътрешните органи (черен дроб, бъбреци и др.) могат да бъдат придружени от полиневропатия, подобна на GBS;
· ЯМР на мозъка *-необходим за диференциална диагноза с патология на централната нервна система (остър мозъчно-съдов инцидент, енцефалит);
ЯМР на гръбначен мозък* - за изключване на лезии (миелит) на ниво цервикално удебеление на гръбначния мозък (C4 - Th2);
Електроневромиография ** (ENMG) - може да бъде нормална през първата седмица на заболяването, с мускулно увреждане, се открива тип денервация на ENMG кривата, импулсната проводимост е бавна, признаци на увреждане на миелина или аксоните. Най-често се изследват дисталните мускули на горните и долните крайници (напр. tibialis anterior, extensor digitorum common), а при необходимост и проксималните мускули (напр. quadriceps femoris).
*NB!
Абсолютни противопоказания за ЯМР са: метално чуждо тяло в орбитата; интракраниални аневризми, клипсирани с феромагнитен материал; електронни устройства в тялото (пейсмейкър); хемопоетична анемия (за контрастиране).
Относителни противопоказания за ЯМР са:
тежка клаустрофобия;
метални протези, щипки, разположени в не-сканирани органи;
Интракраниални аневризми, изрязани с неферомагнитен материал.
** NB! ENMG е единственият инструментален диагностичен метод, който позволява да се потвърдят лезиите на периферната нервна система и съответно диагнозата GBS, както и да се изясни естеството на патологичните промени (демиелинизиращи или аксонални) и тяхното разпространение.
Протоколът и обхватът на ENMG изследванията при пациенти с GBS зависят от клиничните прояви на заболяването:
- при преобладаваща дистална пареза се изследват дълги нерви на ръцете и краката: най-малко 4 моторни и 4 сетивни (моторни и сетивни части на медианния и улнарния нерв; перонеален, тибиален, повърхностен перонеален и сурален нерв от едната страна). Оценяват се основните параметри на ENMG:
моторни реакции (дистална латентност, амплитуда, форма и продължителност), оценява се наличието на блокове на възбуждане и дисперсия на отговорите; анализира се скоростта на разпространение на възбуждането по двигателните влакна в дисталните и проксималните области;
сензорни реакции (амплитуда) и скорост на възбуждане по сетивните влакна в дисталните участъци;
· късни ЕНМГ феномени (F-вълни): анализират се латентност, форма и амплитуда на отговорите, стойност на хронодисперсията, процент на отпадане.
- при наличие на проксимална пареза е задължително допълнително изследване на два къси нерва (аксиларен, мускулно-кожен, феморален и др.) с оценка на параметрите на двигателния отговор (латентност, амплитуда, форма).
Трябва да се помни, че първите признаци на процеса на денервация се появяват не по-рано от 2-3 седмици след началото на заболяването, а признаците на процеса на реинервация - не по-рано от 4-6 седмици.
Диагностични критерии за класически GBSот Asbury A.K. и Cornblath D.R.
въз основа на клинични и лабораторни данни:
наличието на прогресивна двигателна слабост с участие в патологичния процес на повече от един крайник;
арефлексия или тежка хипорефлексия;
Анализ на CSF - наличието в 1 µl цереброспинална течност на не повече от 50 моноцита и / или 2 гранулоцита 2+.
Системата за диагностициране на GBS, критериите за която са формулирани от Националния институт за изследване на неврологични и комуникационни разстройства и инсулт (САЩ):
Задължителни критерии:
прогресивна двигателна слабост в повече от един крайник;
Тежестта на парезата варира от минимална слабост в краката до тетраплегия;
Инхибиране на рефлекси в различна степен.
Спомагателни критерии за диагностика на синдрома:
1. слабостта се увеличава в рамките на 4 седмици от началото на заболяването;
2. относителна симетрия на лезията;
3. лека степен на сетивни нарушения;
4. участие в патологичния процес на черепните нерви;
5. възстановяване;
6. симптоми на вегетативна дисфункция;
7. обичайната липса на фебрилен период в началото на заболяването;
8. повишаване на нивото на протеин в цереброспиналната течност (CSF) 1 седмица след появата на симптомите на заболяването, при условие че броят на мононуклеарните левкоцити обикновено не надвишава 10 клетки на 1 mm3;
9. нарушение на проводимата функция на нервите по време на заболяването в приблизително 80% от случаите;
10. липсата на установени причини за увреждане на периферните нерви, като ефекта на хексакарбон, порфирия, дифтерия, други токсични и инфекциозни заболявания, които имитират GBS.
Признаци, които абсолютно изключват диагнозата GBS:
асиметрия на пареза;
изключително сензорни нарушения;
Устойчиви тазови нарушения
Изразени тазови нарушения;
скорошна дифтерия;
Наличието на психопатологични симптоми - халюцинации, заблуди;
Доказано отравяне със соли на тежки метали и др.
Диагностичен алгоритъм:
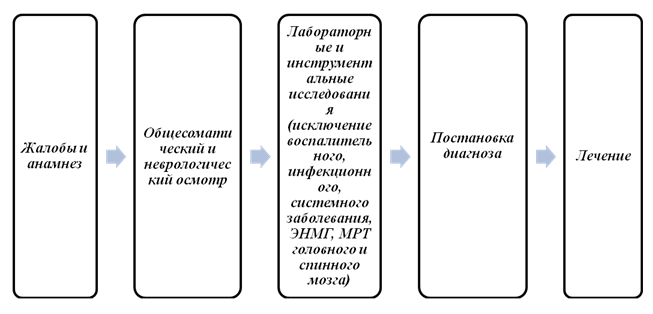
Диагностика (болница)
ДИАГНОСТИКА НА СТАЦИОНАРНО НИВО
Диагностични критерии на болнично ниво:виж амбулаторно ниво.
Оплаквания и анамнеза:виж амбулаторно ниво.
Физическо изследване:виж амбулаторно ниво.
* NB! Критериите, дадени в параграф 9, параграф 1, са характерни за GBS, аксонални, парапаретични и фаринго-цервико-брахиални форми, а такива форми като синдром на Miller Fisher и остра пандизавтономия клинично се различават значително от другите форми на GBS, следователно като цяло приетите критерии за диагностициране на това заболяване са трудни за прилагане. Диагнозата в тези случаи се установява преди всичко въз основа на анамнестичните данни и клиничната картина на заболяването.
Характеристики на синдрома на Милър Фишер.
Зашеметяване, объркване поради хипонатриемия, свързана със свръхпроизводство на антидиуретичен хормон. Конвулсии могат да се появят, когато съдържанието на натрий в плазмата е под 120 mmol / l.
Характеристики на острата пандизавтономия.
появата на неврологични симптоми 1-2 седмици след вирусна или бактериална инфекция;
Наличието на изолирана лезия на автономната нервна система;
Често се засяга сърдечно-съдовата система (постурална хипотония, артериална хипертония, тахикардия, сърдечни аритмии);
замъглено зрение, сухота в очите, анхидроза;
дисфункция на стомашно-чревния тракт (паралитичен илеус);
Трудности при уриниране, остра задръжка на урина;
Повишено изпотяване, синкаво оцветяване на кожата на ръцете и краката, студени крайници;
Зашеметяване, объркване поради хипонатриемия, свързана със свръхпроизводство на антидиуретичен хормон. Конвулсии могат да се появят, когато съдържанието на натрий в плазмата е по-малко от 120 mmol / l;
Възстановяването е постепенно и често непълно.
За да се постави диагноза синдром на Guillain-Barré, е необходимо ясно да се определи историята на развитието на заболяването, заедно с оценка на неврологичния статус, за да се сравни с критериите за диагностициране на GBS (СЗО; 1993). Препоръчително е да се извърши лумбална пункция с изследване на CSF, както и да се потвърди невронното ниво на лезията и да се изясни формата на заболяването според ENMG изследването.
Диагностичен алгоритъм:
GBS трябва преди всичко да се разграничи от състояния, които могат да доведат до развитие на остра периферна тетрапареза. Диференциално диагностичното търсене е значително опростено, когато се използва уникален алгоритъм, разработен от изследователите на Федералната държавна бюджетна институция "NTsN" на Руската академия на медицинските науки.
Диференциално диагностичен алгоритъм за остра вяла тетрапареза (AFT)

Забележка: OBT-остра вяла тетрапареза; ЕМГ електромиография; PNP полиневропатия; GBS - синдром на Guillain-Barré; ЛП - лумбална пункция; BHAK - биохимичен кръвен тест; RF - ревматичен фактор; CRP - С-реактивен протеин; CPK - креатинин фосфокиназа; ЯМР - ядрено-магнитен резонанс (не по-малко от 1 Т); CT - компютърна томография.
Лабораторни изследвания:вижте амбулаторно ниво (към тези изследвания, които са изброени допълнително).
Списък на основните лабораторни изследвания:
кръв за имуноглобулини - при планиране на специфична терапия с имуноглобулини от клас G е необходимо да се определят Ig фракции в кръвта, ниската концентрация на IgA обикновено се свързва с неговия наследствен дефицит, в такива случаи съществува висок риск от развитие на анафилактичен шок ( имуноглобулинова терапия е противопоказана);
Изследване на CSF (цитоза, концентрация на протеин). При анализиране на цереброспиналната течност следните три показателя обикновено се приписват на броя на диагностичните критерии, потвърждаващи GBS:
Наличието на високо съдържание на протеини,
повишаване на фракцията на албумин,
Няма съпътстващо повишаване на цитозата.
Освен това могат да се препоръчат следните диагностични тестове за потвърждаване на диагнозата и изясняване на характеристиките на GBS в конкретен случай:
· кръвен тест за автоантитела към ганглиозиди, със задължително изследване на GM1, GD1a и GQ1b, ако пациентът има окуломоторни нарушения;
кръвен тест за IgA антитела към Campylobacter jejuni;
· изследване на съдържанието на биомаркери на тежки вериги на неврофиламент, тау-протеин и глиофибриларен кисел протеин в кръвния серум.
Инструментални изследвания: вижте амбулаторно ниво.
При тежки случаи на заболяването (бърза прогресия, булбарни нарушения) 24-часово мониториране на кръвното налягане, ЕКГ, пулсова оксиметрия и изследване на функцията на външното дишане (спирометрия, пикфлоуметрия), мониториране на функцията на външното дишане (определяне на жизнения капацитет на белите дробове (VC) трябва да се извърши (в условията на интензивното отделение). ) за навременно идентифициране на индикации за прехвърляне на пациента към механична вентилация.
Диференциална диагноза
GBS трябва да се диференцира от други заболявания, проявяващи се с остра периферна пареза, предимно от полиомиелит (особено при малки деца) и други полиневропатии (дифтерия, с порфирия). В допълнение, лезиите на гръбначния мозък и мозъчния ствол (напречен миелит, инсулт във вертебробазиларната система) и заболявания с нарушена нервно-мускулна трансмисия (миастения гравис, ботулизъм) могат да имат подобна клинична картина.
|
Диагноза |
Обосновка на диференциалната диагноза |
Проучвания |
Критерии за изключване диагноза |
| Полиомиелит (особено при малки деца) | Остра периферна пареза |
· ЕНМГ; игла ЕМГ; консултация с терапевт; консултация инфекционист. |
епидемиологична история; Наличие на треска в началото на заболяването; симптоми на стомашно-чревния тракт; асиметрия на лезията; липса на обективни нарушения на чувствителността; висока цитоза в цереброспиналната течност; Диагнозата полиомиелит се потвърждава чрез вирусологично или серологично изследване. |
|
Други полиневропатии (възпалителни: хронична възпалителна полиневропатия с остро начало, болест на Sjögren, болест на Churg-Strauss, криоглобулинемичен васкулит; Инфекциозни: HIV-асоциирани, лаймска болест; Токсичен: дифтерия, порфирия, наркотици, остър алкохол, отравяне с тежки метали Дисметаболитни: полиневропатия на критични състояния, с бъбречна, чернодробна недостатъчност, остра хипергликемична полиневропатия) |
Остра периферна пареза |
· ЕНМГ; игла ЕМГ; · минуси.терапевт; · конс.нфектионист; биохимични изследвания на кръв и урина |
признаци на текущия процес на денервация-реинервация; Комбинацията от предимно моторна полиневропатия с тежка коремна болка, чревна пареза, артериална хипертония, тахикардия, тежки психични промени (от депресия до делириум), нарушение на съня и епилептични припадъци свидетелства в полза на порфирия. припорфирията има промяна в цвета на урината, която става червеникава на светлина, а след това в богат червеникаво-кафяв цвят |
|
Трансверзален миелит.Увреждане на нивото на цервикалното удебеляване на гръбначния мозък (C4 - Th2) постинфекциозен (M.pneumoniae, Schistosoma), след ваксинация, вирусен (ентеровируси, херпес), HIV-свързан миелит, с демиелинизиращи заболявания на централната нервна система, със системни заболявания (системен червен лупус, болест на Sjögren, остър некротичен васкулит) |
Остра периферна пареза |
· ЯМР на гръбначен и главен мозък; · ЕНМГ; минуси терапевт; минуси.инфекционист. |
Сегментна граница на сензорно увреждане; Устойчиви тазови нарушения Липса на участие на мимически и дихателни мускули при тежка тетрапареза. |
|
Остро нарушение на спиналното кръвообращение в вертеберо-базиларния басейн. (тромбоза на съдовете на гръбначния мозък, съдова малформация, аневризма, компресия, травма, неоплазма на гръбначния мозък) |
Остра периферна пареза |
· ЯМР на главен и гръбначен мозък; · ЕНМГ; минуси терапевт; минуси неврохирург. |
остро развитие (обикновено в рамките на няколко минути); В повечето случаи потискане на съзнанието (кома); Окончателната диагноза се потвърждава с ЯМР на главния/гръбначния мозък. |
| Миастения гравис | Остра периферна пареза | ENMG. |
Променливостта на симптомите липса на сензорни нарушения; характерни промени в сухожилните рефлекси; Диагнозата се потвърждава от ЕМГ (откриване на феномен на намаляване); положителен фармакологичен тест с прозерин. |
| Ботулизъм | Остра периферна пареза |
· ЕНМГ; минуси.инфекционист. |
Съответни епидемиологични данни Низходящ тип разпространение на пареза, Запазване по отношение на случаи на сухожилни рефлекси, липса на сензорни нарушения, няма промяна в това даликворе. |
Лечение в чужбина
Лекувайте се в Корея, Израел, Германия, САЩ
Лечение в чужбина
Получете съвет за медицински туризъм
Лечение
Лекарства (активни вещества), използвани при лечението
Лечение (амбулаторно)
ЛЕЧЕНИЕ НА АМБУЛАТОРНО НИВО
Тактика на лечение:
Подозрението за синдром на Guillain-Barré, дори при минимални симптоми, е основа за спешна хоспитализация, а симптоматичното лечение се извършва на амбулаторния етап и когато диагнозата се установи, те се изпращат в болницата, а пациентът и неговите роднини трябва да бъдат предупредени за възможно бързо влошаване на състоянието.
Нелекарственлечение:не.
Медицинско лечение:
Симптоматична терапия:
При повишаване на кръвното налягане може да се предпише нифедипин, 10-20 mg под езика;
За намаляване на тахикардията се използва пропраналол в начална доза от 20 mg 3 пъти на ден; след това дозата постепенно се увеличава до 80-120 mg в 2-3 приема, под контрола на кръвното налягане, сърдечната честота, ЕКГ;
В случай на брадикардия - атропин, за възрастни: IV болус под контрола на ЕКГ и кръвно налягане - 0,5-1 mg, ако е необходимо, въвеждането се повтаря след 3-5 минути; максималната доза е 0,04 mg/kg (3 mg). Деца - 10 mcg / kg;
за намаляване на болката се прилагат аналгетици, нестероидни противовъзпалителни средства:
Кеторолак, перорално еднократно в доза от 10 mg или многократно, в зависимост от тежестта на синдрома на болката, 10 mg до 4 пъти на ден. Максималната дневна доза не трябва да надвишава 40 mg или не повече от 60 mg се прилага интрамускулно за 1 инжекция; обикновено 30 mg на всеки 6 часа.
диклофенак, интрамускулно. Единична доза е 75 mg, максималната дневна доза е 150 mg (с прекъсване между инжекциите от най-малко 30 минути).
ибупрофен, 1-2 таблетки 3-4 пъти на ден; при необходимост - по 1 таблетка на всеки 4 часа. Не приемайте по-често от след 4 часа. Максималната дневна доза за възрастни не трябва да надвишава 1200 mg (не повече от 6 таблетки за 24 часа).
Алгоритъм за действие при извънредни ситуации:мерки за симптоматично лечение.
Други видове лечение:не.
консултация с инфекционист - установяване или изключване на инфекциозно заболяване (инфекциозна мононуклеоза, лаймска болест, ХИВ и др.);
консултация с терапевт - установяване или изключване на терапевтично заболяване (възпалително заболяване на вътрешните органи: бели дробове, бъбреци, черен дроб и др.);
консултация с ендокринолог, нефролог, ревматолог - при необходимост изключване на соматична патология.
Превантивни действия:
Няма специфична превенция на заболяването, лекарите могат да препоръчат лечение на всички инфекциозни заболявания в самото начало на тяхното развитие, това ще намали отрицателното въздействие на патогените върху нервната система.
Мониторинг на пациента:
оценка на общото състояние на пациента с описание на състоянието на кожата; тегло на пациента;
хемодинамични параметри: брой дихателни движения, A/D, сърдечна честота, пулс;
оценка на неврологичния статус.
На този етап не се провежда етиопатогенетично лечение, поради което липсват показатели.
Лечение (линейка)
ДИАГНОСТИКА И ЛЕЧЕНИЕ В СПЕШЕН СТАДИЙ
Диагностични мерки:
Често GBS има остър ход и е потенциално животозастрашаващ, тъй като, започвайки от краката, лезията прогресира, разпространява се до булбарните и други черепни нерви, поради което са необходими следните мерки:
Резултат при преглъщане- с булбарна парализа, нарушение на преглъщането, за предотвратяване на аспирация
назогастрална сонда.
Оценка на дишането- възможно е развитието на прогресивна дихателна недостатъчност и не само от обструктивен тип поради булбарна парализа, но и с увреждане на диафрагмалния нерв (характерен е парадоксален тип дишане - при вдишване предната коремна стена потъва) и междуребрие.
Трахеална интубация (за по-нататъшно прехвърляне на пациента към механична вентилация).
Оценка на работата на сърцето:
· ЕКГ -намаляване и дори инверсия на S-T сегмента, увеличаване на Q-T интервала, възможно е сърдечен арест.
По време на транспортирането е важно да се грижи за поддържането на проходимостта на дихателните пътища, внимателно да се следи кръвното налягане и сърдечната честота, тахикардия, ортостатична хипотония, аритмия и др.
Медицинско лечение:
Посиндромна терапия съгласно протокола за оказване на спешна медицинска помощ.
Лечение (болнично)
ЛЕЧЕНИЕ НА СТАЦИОНАРНО НИВО
Тактика на лечение:Основната цел на лечението е: възстановяване на жизнените функции, елиминиране на симптомите на автоимунно заболяване с помощта на специфични техники, период на рехабилитация на пациента и предотвратяване на усложнения. Първото нещо, което трябва да направите, е да поставите пациента в болница и, ако е необходимо, да го свържете към белодробен вентилатор, да инсталирате катетър, ако има нарушение на отделянето на урина, и да инсталирате назогастрална сонда, ако преглъщането е затруднено.
Нелекарствено лечение:
При тежки случаи с тежка пареза правилното лечение е от особено значение за предотвратяване на усложнения, свързани с продължителна неподвижност на пациента (инфекции, рани от залежаване, белодробна емболия). Необходима е периодична (поне веднъж на всеки 2 часа) смяна на позицията на пациента, грижа за кожата, контрол на функциите на пикочния мехур и червата, пасивна гимнастика, профилактика на аспирация. При персистираща брадикардия заплахата от асистолия може да изисква инсталирането на временен пейсмейкър.
Медицинско лечение:
Специфична терапия за синдрома на Guillain-Barré, насочена към спиране на автоимунния процес, понастоящем се използва пулсова терапия с имуноглобулини от клас G и плазмафереза (виж параграф - други видове лечение). Ефективността на всеки от методите е относително еднаква, така че едновременното им използване се счита за неподходящо.
Имуноглобулин клас G, подобно на плазмаферезата, намалява продължителността на престоя на механична вентилация; прилага се венозно дневно в продължение на 5 дни в доза 0,4 g/kg. Възможни нежелани реакции: гадене, главоболие и болки в мускулите, треска.
Симптоматичната терапия за синдрома на Guillain-Barré се провежда за коригиране на нарушенията на киселинно-алкалния и водно-електролитния баланс, коригиране на нивата на кръвното налягане и предотвратяване на дълбока венозна тромбоза на тромбоемболия.
Инфузионна терапия за корекция на нарушения на киселинно-базовия, водно-електролитния баланс, тежка артериална хипотония.
При персистираща тежка хипертония се предписват антихипертензивни лекарства (бета-блокери или бавни блокери на калциевите канали) (виж CP Хипертония).
При тежка тахикардия се предписват β-блокери (пропранолол), при брадикардия - атропин (виж по-долу).
При развитието на интеркурентни инфекции е необходима антибиотична терапия (използват се широкоспектърни лекарства).
За профилактика на дълбока венозна тромбоза и белодробна емболия се предписва нискомолекулен хепарин в профилактични дози два пъти дневно).
При болка от ноцицептивен произход (мускулна, механична) се препоръчват НСПВС, при невропатична болка лекарствата на избор са габапентин, карбамазепин, прегабалин (само за възрастни!) (виж по-долу).
Списък на основните лекарства:.
| Препарати | единична доза | Множество въвеждане |
| Имуноглобулин клас G | 0,4 g/kg IV. | . 0,4 g/kg/ден в продължение на 5 дни веднъж дневно, 5 дни. |
| габапентин | 300 мг |
Ден 1 300 mg 1 път / ден, Ден 2 300 mg 2 пъти / ден, Ден 3 300 mg 3 пъти / ден, след това, в зависимост от индивидуалната поносимост и ефективност, дозата може да се увеличи с 300 mg / ден на всеки 2-3 дни до максимум 3600 mg / ден. |
| карбамазепин | 200 мг | Препоръчителната начална доза е 200-400 mg на ден. Дозата може постепенно да се увеличава до постигане на задоволителен клиничен ефект, в някои случаи може да бъде 1600 mg на ден. След като синдромът на болката премине в ремисия, дозата може постепенно да се намали. |
| прегабалин | 150 мг | Лечението започва с доза от 150 mg на ден, разделена на два или три приема. В зависимост от индивидуалния отговор на пациента и поносимостта, след 3-7 дни дозата може да се увеличи до 300 mg дневно, а при необходимост след още 7 дни - до максимална доза от 600 mg дневно. |
Списък на допълнителни лекарства:.
| Препарати | единична доза | Множество въвеждане |
| нифедипин | 10 мг | 1-2 пъти под езика |
| пропранолол | 10 мг | 20 mg 3 пъти / ден, след което дозата постепенно се увеличава до 80-120 mg в 2-3 дози, под контрола на кръвното налягане, сърдечната честота, ЕКГ |
| Атропин | 0,5-1,0 | възрастни: интравенозен болус под контрола на ЕКГ и кръвно налягане - 0,5-1 mg, ако е необходимо, въвеждането се повтаря след 3-5 минути; максималната доза е 0,04 mg/kg (3 mg). Деца - 10 mcg / kg .; |
| Кеторолак | 10 мг | перорално веднъж в доза от 10 mg или многократно, в зависимост от тежестта на синдрома на болката, 10 mg до 4 пъти на ден. Максималната дневна доза не трябва да надвишава 40 mg или не повече от 60 mg се прилага интрамускулно за 1 инжекция; обикновено 30 mg на всеки 6 ч. Не се използва при деца. |
| диклофенак | 75 мг | интрамускулно, единична доза от 75 mg, максималната дневна доза е 150 mg (с прекъсване между инжекциите от най-малко 30 минути). Децата не се прилагат. |
| ибупрофен | 0,2 гр |
1-2 таблетки 3-4 пъти дневно; при необходимост - по 1 таблетка на всеки 4 часа. Не приемайте по-често от след 4 часа. Максималната дневна доза за възрастни не трябва да надвишава 1200 mg (не повече от 6 таблетки за 24 часа). Деца: 10-20 mg/kg 3 пъти дневно в продължение на 2-3 дни. |
Хирургична интервенция, посочваща индикации за хирургична интервенция: Може да се наложи хирургична интервенция за трахеостомия при продължителна механична вентилация (повече от 10 дни), както и гастростомия при тежки и продължителни булбарни нарушения.
Други видове лечение:
Винаги трябва да помните изключителното значение на комплекс от рехабилитационни мерки за предотвратяване на усложнения, дължащи се на неподвижност на пациента и за поддържане на функционалното състояние на мускулите, докато се появи достатъчен обем независими движения.
Пациентът се нуждае от:
- Физиотерапия
- Масажът има благоприятен ефект върху метаболизма, което също така ускорява растежа и реинервацията на нервите
- Физиотерапия за предотвратяване образуването на контрактури (електрическа стимулация, топлинна обработка, лекарствена електрофореза и др.).
- Хипербарна кислородна терапия.
Мембранната плазмафереза значително намалява тежестта на парезата и продължителността на механичната вентилация. Като правило се провеждат 4-6 сесии с интервал от един ден; обемът на плазмата, която трябва да бъде заменена за една сесия, трябва да бъде най-малко 40 ml/kg. Като заместителна среда се използва 0,9% разтвор на натриев хлорид или реополиглюкин.
Трябва да се помни за противопоказанията за плазмафереза (инфекции, нарушения на кръвосъсирването, чернодробна недостатъчност), както и за възможните усложнения (нарушение на електролитния състав, хемолиза, алергични реакции).
Показания за експертен съвет:
консултация със специалист по инфекциозни заболявания, ако е необходимо (при липса на специалист на доболнично ниво) - установяване или изключване на хронична инфекция (бруцелоза, борелиоза и др.), както и в случай на потвърждение на инфекциозен агент правилна етиологична терапия;
консултация с терапевт при необходимост (при липса на специалист на доболнично ниво) - установяване или изключване на терапевтично заболяване (възпалително заболяване на вътрешните органи: бели дробове, бъбреци, черен дроб и др.), корекция на хемодинамичните параметри, електролит баланс по време на терапията;
консултация с лекар на интензивно отделение - лечението на пациенти с тежки форми на синдрома на Guillain-Barré се извършва съвместно с лекаря на отделението за интензивно лечение;
консултация с кардиолог - при тежки сърдечно-съдови нарушения (упорита тежка артериална хипертония, аритмии).
Показания за прехвърляне в интензивно отделение и реанимация:
Тежка и изключително тежка степен на неврологични разстройства;
хемодинамична нестабилност;
нарушение на дихателната функция.
Индикатори за ефективност на лечението:
Стабилизиране на имунологичния статус (количествен и качествен състав на IgG кръв и цереброспинална течност);
Регресия на фокалните неврологични симптоми.
По-нататъшно управление.
След нормализиране на здравословното състояние на пациента, той трябва да бъде регистриран при невролог. Освен това ще е необходимо да се подложат на превантивни прегледи, за да се идентифицират предпоставките за рецидив на заболяването на ранен етап. Диспансерно наблюдение в клиниката по местоживеене.
След края на острия период са необходими комплексни рехабилитационни мерки, чийто план се изготвя индивидуално, в зависимост от тежестта на остатъчните симптоми (ЛФК, масаж, докато топлинните процедури са противопоказани!).
Пациенти с GBS. трябва да бъдат информирани за необходимостта от спазване на защитния режим най-малко 6-12 месеца след края на заболяването. Физическо претоварване, прегряване, хипотермия, прекомерна инсолация, прием на алкохол са неприемливи. Също така през този период трябва да се въздържате от ваксинация.
медицинска рехабилитация
се извършва в съответствие със Стандарта за организация на медицинската рехабилитация на населението на Република Казахстан, одобрен със заповед на министъра на здравеопазването на Република Казахстан от 27 декември 2013 г. № 759.
Палиативна грижа
В зависимост от вида и тежестта на усложненията след заболяването може да се наложи допълнително лечение, като например:
Имобилизираните пациенти получават хепарин подкожно в доза от 5000 IU на всеки 12 часа и временно притискане на мускулите на прасеца за предотвратяване на дълбока венозна тромбоза;
масажът има благоприятен ефект върху метаболизма, което също ускорява растежа на нервите и реинервацията;
кинезитерапията доказано стимулира реинервацията и възстановява мускулния обем;
физиотерапия за подобряване на силата, за предотвратяване на образуването на контрактури (електрическа стимулация, топлинна терапия, лекарствена електрофореза);
· рехабилитация за развитие на ежедневни умения и използване на адаптивни продукти, които помагат в ежедневието;
Пациентът може да се нуждае от ортопеди или други помощни устройства за подобряване на движението.
психотерапия;
Хоспитализация
Показания за планирана хоспитализация:не.
Показания за спешна хоспитализация:
Пациентите с GBS подлежат на хоспитализация в интензивното отделение.
Информация
Извори и литература
- Протоколи от заседанията на Съвместната комисия по качеството на медицинските услуги на MHSD RK, 2016 г.
- 1. Бикова О. В., Бойко А. Н., Маслова О. И. Интравенозно използване на имуноглобулини в неврологията (Преглед на литературата и собствени наблюдения) // Nevrol. списание - 2000, 5. С.32-39. 2. Гехт Б. М., Меркулова Д. М. Практически аспекти на клиниката и лечението на полиневропатия // Nevrol. сп.-1997.-No2.-C.4-9. 3. Пирадов М.А., Супонева Н.А. Синдром на Гилен-Баре: Диагностика и лечение. Ръководство за лекари” -2011г. 4. Супонева Н.А., Пирадов М.А. "Интравенозна имунотерапия в неврологията" -2013г. 5. Sladky J. T. Синдром на Guillain-Barre при деца // J. Child Neurol. 2004. Т. 19. С. 191–200. 6. Schmidt B., Toyka K. V., Kiefer R. et al. Възпалителни инфилтрати в биопсии на сурален нерв при синдром на Guillain-Barre и хронична възпалителна демиелинизираща невропатия // 1996. V. 19. P. 474–487. 7. Khalili-Shirazi A., Hughes R. A., Brostoff S. W. et al. Т-клетъчни отговори на миелинови протеини при синдром на Guillain-Barre // J. Neurol. наука 1992. Т. 111. С. 200–203. 8. Van Rhijn I., Bleumink-Pluym N.M., Van Putten J.P. et al. ДНК на Campylobacter присъства в циркулиращи миеломоноцитни клетки на здрави хора и при хора със синдром на Guillain-Barre // J. Infect. дис. 2002. Т. 185. С. 262–265. 9. Купър J.C., Ben-Smith A., Savage C.O. et al. Необичайно използване на ген на фенотип V на Т-клетъчен рецептор на гама делта Т-клетки в линия, получена от периферен нерв на пациент със синдром на Guillain-Barre // J. Neurol. неврохирургия. Психиатрия. 2000. Т. 69. С. 522–524. 10. Иляс А. А., Чен З. У., Кук С. Д. и др. Разпределение на подклас на имуноглобулин G на автоантитела към ганглиозиди при пациенти със синдром на Guillain-Barre // Res. общ. Патол. Pharmacol. 2002. Т. 109. С. 115–123. 11. Tsang R. S., Valdivieso-Garcia A. Патогенеза на синдрома на Guillain-Barre // Expert Rev. Против инфекции. Там. 2003. Т. 1. С. 597–608. 12. Kieseier B.C., Kiefer R., Gold R. et al. Напредък в разбирането и лечението на имуномедиирани разстройства на периферната нервна система // Мускулен нерв. 2004. Т. 30. С. 131–156. 13. Адамс Д., Гибсън Дж. Д., Томас П. К. и др. HLA антигени при синдром на Guillain-Barre // Lancet. 1977. № 2. С. 504–505. 14. Кога М., Юки Н., Кашивасе К. и др. Синдромите на Guillain-Barre и Fisher след Campylobacter jejuni ентерит са свързани с HLA-54 и Cwl, независимо от анти-ганглиозидни антитела // J. Neuroimmunol. 1998. Т. 88. С. 62–66. 15. Magira E.E., Papaijakim M., Nachamkin I. et al. Диференциално разпределение на HLA-DQ бета/DR бета епитопи при двете форми на синдрома на Guillain-Barre, остра моторна аксонална невропатия и остра възпалителна демиелинизираща полиневропатия (AIDP); идентифициране на DQ бета епитопи, свързани с чувствителност към и защита от AIDP // J. Immunol. 2003. Т. 170. С. 3074–3080. 16. Geleijns K., Schreuder G.M., Jacobs B.C. et al. HLA клас II алелите не са общ фактор на чувствителност при синдрома на Guillain-Barre // Неврология. 2005. Т. 64. С. 44–49. 17. Asbury A. K., Cornblath D. R. Оценка на настоящите диагностични критерии за синдрома на Guillain-Barre // Ann. неврол. 1990. Т. 27. С. 21–24.
Информация
ИЗПОЛЗВАНИ СЪКРАЩЕНИЯ В ПРОТОКОЛА
| CIDP | хронична възпалителна демиелинизираща полирадикулоневропатия |
| PNP | полиневропатия |
| НДСВ | наследствена моторно-сензорна полиневропатия |
| SGB | Синдром на Guillain-Barré |
| ПО дяволите | артериална хипертония |
| PNS | периферна нервна система |
| ЦНС | Централна нервна система |
| ЯМР | Магнитен резонанс |
| PCR | полимеразна верижна реакция |
| CSF | гръбначно-мозъчна течност |
| СУЕ | скорост на утаяване на еритроцитите |
| Иг | имуноглобулин |
| сърдечен ритъм | сърдечен ритъм |
| СПИН | синдром на придобита имунна недостатъчност |
| ЕМГ | електромиография |
| ENMG | електроневромиография |
| IVIG | нормален човешки имуноглобулин за интравенозно приложение |
| GC | глюкокортикоиди |
Списък на разработчиците на протоколи с квалификационни данни:
1. Кайшибаева Гульназ Смагуловна, кандидат на медицинските науки, АО "Казахстански медицински университет за продължаващо обучение", ръководител на катедрата по неврология, сертификат "възрастен невропатолог".
2. Жумагулова Кулпарам Габибуловна, кандидат на медицинските науки, сертификат "възрастен невропатолог от най-висока категория", АО "Казахстански медицински университет за продължаващо обучение", доцент на катедрата по неврология.
3. Тулеутаева Райхан Йесенжановна, клиничен фармаколог, кандидат на медицинските науки, професор на Руската академия по естествени науки, ръководител на катедрата по фармакология и медицина, основана на доказателства, Държавен медицински университет Семей.
Индикация за липса на конфликт на интереси:не.
Списък на рецензенти:
Душанова Г.А. - доктор на медицинските науки, професор, ръководител на катедрата по неврология, психиатрия и психология на Южноказахстанската държавна фармацевтична академия.
Посочване на условията за преразглеждане на протокола:Ревизия на протокола 3 години след публикуването му и от датата на влизането му в сила или ако има нови методи с ниво на доказателства.
Прикачени файлове
внимание!
- Като се самолекувате, можете да причините непоправима вреда на здравето си.
- Информацията, публикувана на уебсайта на MedElement, не може и не трябва да замества личната медицинска консултация. Не забравяйте да се свържете с медицинските заведения, ако имате някакви заболявания или симптоми, които ви притесняват.
- Изборът на лекарства и тяхната дозировка трябва да се обсъди със специалист. Само лекар може да предпише правилното лекарство и неговата дозировка, като вземе предвид заболяването и състоянието на тялото на пациента.
- Уебсайтът на MedElement е само информационен и справочен ресурс. Информацията, публикувана на този сайт, не трябва да се използва за произволна промяна на лекарските предписания.
- Редакторите на MedElement не носят отговорност за каквито и да било вреди за здравето или материални щети в резултат на използването на този сайт.
Синдромът на Guillain-Barré е група от остри, бързо прогресиращи автоимунни заболявания, при които атаката е насочена към клетките на Шван и миелина, които образуват обвивката на нервните влакна. Синдромът се проявява с вяла пареза, сензорни нарушения, вегетативни нарушения. Развива се 1-3 седмици след инфекция на стомашно-чревния тракт или дихателните пътища, така че се смята, че автоимунната реакция в някои случаи се отключва от прекарано заболяване. Синдромът причинява тежки усложнения, които преди са били фатални. Но благодарение на съвременните методи на интензивно лечение, смъртността е намаляла до 5%.
Причините
Точните причини за синдрома на Гилен-Баре не са установени, но има няколко хипотези за произхода на заболяването.
- Черепно-мозъчна травма. Физическото увреждане води до подуване на мозъка и появата на тумори в него. Синдромът може да бъде далечна последица от това, следователно диагнозата взема предвид TBI в анамнезата.
- Инфекция. Много пациенти имат признаци на респираторна и стомашно-чревна инфекция 1 до 3 седмици преди появата на симптомите на синдрома. Следователно е вероятно прехвърленото заболяване да предизвика автоимунна реакция. В този аспект патологичната роля се отрежда на Campylobacter jejuni, който причинява ентерит, херпесни вируси, микоплазми, Haemophilus influenzae, HIV инфекция. Подобна роля могат да играят хирургични интервенции, ваксинации, наранявания на периферните нерви.
- наследствено предразположение. В рисковата зона попадат пациенти, в чието семейство има случаи на синдрома. При утежнена наследственост, както нараняване на главата, така и инфекциозни заболявания често служат като задействащ фактор.
Класификация
В зависимост от симптомите и засегнатата област, синдромът на Guillain-Barré може да приеме класическа, аксонална, атипична форма или да се изрази като синдром на Miller-Fischer.
Класическата форма се наблюдава в 80% от случаите и представлява възпалително-демиелинизираща полирадикулоневропатия. Аксоналната форма се среща в 15% от случаите, при нея има двигателна или моторно-сензорна невропатия с увреждане на аксоните на нервните влакна, отговорни за движението и чувствителността на мускулите. При синдрома на Милър-Фишер, който се наблюдава в 3% от случаите, има парализа на мускулите на окото, липса на един или повече рефлекси, лека пареза и нарушена координация и двигателни умения. При атипичната форма, която е изключително рядка, има сензорна и автономна невропатия, както и краниална полиневропатия.
Според продължителността на периода на нарастване на симптомите, синдромът се разделя на остра форма (7-14 дни), подостра (15-28 дни) и хронична (до няколко месеца с периоди на ремисия и влошаване). Последният се счита за най-тежък, тъй като е по-труден за диагностициране и намалява шансовете за навременно лечение.
Симптоми
Симптомите на синдрома на Guillain-Barré първоначално са подобни на тези на вирусна респираторна инфекция. Телесната температура се повишава рязко, наблюдава се възпаление на горните дихателни пътища, пациентът чувства обща слабост и болки в ставите. Понякога се отбелязват стомашно-чревни смущения.
Синдромът се различава от ARVI със слабост на крайниците, намаляване и загуба на чувствителност. Първоначално дискомфортът се появява в долната част на краката, след това се разпространява към краката, засяга пръстите на краката. Има изтръпване в ставите на пръстите, а болки се редуват с изтръпване. С напредването на болестта се губи контрол върху малки прости движения, например става трудно да се пише на ръка. Симптомите се появяват симетрично в крайниците.
Друг характерен признак е забележимо увеличение на корема. Поради факта, че дишането е напълно преустроено от горния към коремния тип, стомахът изпъква забележимо напред. Диафрагмата отслабва, дишането с белите дробове става все по-трудно.
Когато мускулите на фаринкса са включени в патологичния процес, тяхното отслабване предотвратява нормалното преглъщане. Пациентът може да се задави от собствената си слюнка. Поради отслабването на мускулите на устата му е трудно да дъвче и да яде. Поради синдрома пациентът има лош контрол върху задържането на урина и чревните газове. Синдромът засяга почти всички вътрешни органи, причинявайки тахикардия, хипертония, замъглено зрение и други прояви.
Симптомите на синдрома на Guillain-Barré най-често се влошават в продължение на няколко седмици. Всичко започва с лека слабост в крайниците и води до изразени нарушения. Това е изпълнено с ненавременна диагноза и усложнения в бъдеще. В острата форма на заболяването парализата може да обхване по-голямата част от тялото след един ден. Първоначално има изтръпване на крайниците, слабост в раменете, гърба, таза. След няколко часа се забелязва очевидно затруднено дишане. Пациентът трябва спешно да бъде откаран в лечебно заведение, където може да му бъде оказана помощ, включително свързан към вентилатор.
Без лечение синдромът води до усложнения, при които рискът от смърт е висок. Това е парализа на мускулите на дихателните и булбарните групи, очните мускули, диафрагмата, корема, гърба, както и пневмония, тромбоемболия, сърдечен арест, сепсис.
Диагностика
Диагнозата на синдрома включва снемане на анамнеза (текущи симптоми, скорошни наранявания, ТОРС, стомашно-чревни нарушения, ваксинация играят голяма роля). Извършва се неврологичен преглед за откриване на сензорни и двигателни нарушения, както и лабораторни изследвания (серологични, общи и биохимични изследвания на кръв и урина).
Ако се подозира синдром, е показано изследване на цереброспиналната течност чрез лумбална или тилна пункция. Ако се открие висока концентрация на протеин (3–5 g/l), това потвърждава диагнозата. При тежки случаи на заболяването се проследява работата на сърдечно-съдовата и дихателната система.
Синдромът може да има признаци, подобни на порфирия, ботулизъм, исхемичен инсулт, миастения гравис, полиомиелит, мозъчно заболяване, парализа, причинена от антибиотици. Диагнозата "синдром на Гилен-Баре" се отхвърля, ако парезата е асиметрична, нарушенията са само сензорни, има персистиращи или тежки тазови нарушения, ако има анамнеза за скорошна дифтерия, халюцинации, заблуди или доказано отравяне с тежки метали соли.
Лечение
Синдромът на Guillain-Barré се лекува в болнични условия. Пациентът се нуждае от подходяща грижа, апаратно наблюдение, лекарствена терапия, в някои случаи спешна операция.
Лекарствената терапия е насочена към спиране на автоимунната реакция. На пациента са показани имуноглобулини от клас G, които се прилагат интравенозно. Те имат странични ефекти като гадене, треска и главоболие, но подобряват дихателната функция. Извършва се и мембранна плазмафереза, при която кръвната плазма на пациента се замества с хлориден разтвор или преполинлюкин. Това намалява тежестта на парезата и намалява времето за поддържане на пациента на вентилатора.
От симптоматичното лечение на синдрома на Guillain-Barré се предписват витамини от група B, антихистамини, антипиретици и болкоуспокояващи, регулатори на сърдечната честота и налягане, антитромбични и антихолинестеразни средства и изкуствени сълзи.
При продължителни булбарни нарушения и развитие на дихателна недостатъчност е възможна трахео- или гастростомия. Слабостта и парализата на дихателните и булбарните мускули изискват наблюдение на дихателната активност, сърдечната честота и кръвното налягане. Понякога е необходим пейсмейкър, с намаляване на белодробния капацитет с 25-30%, е показано използването на вентилатор. Булбарната парализа изисква поставянето на назогастрална сонда. Може също да се наложи да поставите катетър в пикочния мехур.
Грижата за пациента включва профилактика на усложнения, свързани с обездвижването (рани под налягане, тромбоза и др.). За целта положението на тялото на пациента се сменя на всеки 2 часа. Предписва се почистване на кожата, пасивна гимнастика, контрол на работата на червата и пикочния мехур.
Рехабилитация
Прогнозата на заболяването като цяло е положителна: 70% от пациентите се възстановяват напълно, 15% имат пареза и парализа, при които пациентът се признава за инвалид. В 5% от случаите заболяването може да бъде фатално, рискът е повишен при деца и възрастни хора.
Приблизително 2-5% от случаите са свързани с прехода на острата форма на заболяването към хронична рецидивираща. Ето защо е важно не само да следвате всички препоръки на лекаря, но и да положите усилия на етапа на рехабилитация. При синдрома на Guillain-Barré това може да отнеме няколко месеца или години. Пациентите се научават да ходят отново, да използват прибори за хранене, канцеларски материали. Мерките за възстановяване включват масаж, лечебна гимнастика, контрастни душове, вани с радон и сероводород, озокеритна терапия, парафинови вани, електрофореза, магнитотерапия, диета с високо съдържание на витамини В, калций, магнезий и калий.
Пациент, който е претърпял синдрома, трябва редовно да се подлага на електроневромиография, за да оцени динамиката на състоянието. Също така са необходими прегледи от невролог, което ще намали риска от рецидив. В рамките на 12 месеца след началото на заболяването е забранено да се ваксинират.
Запишете се за среща с лекаря
Пирадов М.А. 2000 г
Възможна е рехабилитация
Това заболяване има най-малко осем различни имена - синдром на Ландри (на името на френския невролог, който го описва за първи път през 1859 г.), синдром на Гилен-Баре-Строл (учени, които имат значителен принос в изследването на заболяването), остър полирадикулоневрит и др. Днес според Международната класификация на болестите официално се нарича синдром на Гилен-Баре (GBS) или остра постинфекциозна полиневропатия. В неврологията GBS се счита за уникално заболяване. И не толкова поради относителната си рядкост (среща се при 2 души на 100 000 от населението), а поради възможността за пълна рехабилитация на пациента, въпреки че понякога GBS може да се сравни с най-сериозните заболявания по отношение на тежестта на лезията. Повече разказва заместник-директорът по науката на Научно-изследователския институт по неврология на Руската академия на медицинските науки, ръководител на отделението по неврореанимация, професор Михаил ПИРАДОВ. Синдромът на Guillain-Barré е най-честата причина за остра периферна тетрапареза и парализа. Неврологичните симптоми се развиват много бързо, докато не само двигателните, но и сензорните функции (предимно ставно-мускулната чувствителност) са нарушени, а понякога и много грубо, а сухожилните рефлекси намаляват до пълно изчезване. Тазовите нарушения не са характерни за GBS, но в една трета от случаите дихателната и гълтателната мускулатура са сериозно засегнати. В тежки случаи при лекаря се появява човек, който лежи неподвижно в леглото, който изобщо не може да диша, да преглъща и дори да отвори очите си. Но ако се направи електроенцефалограма на пациент, тя ще бъде същата като на здрав човек, а като човек той не е интелектуално променен ни най-малко. В 70 процента. случаите на GBS се появяват няколко дни след появата на грипоподобни симптоми: умерена температура, мускулни болки, хрема - всичко, което обикновено се нарича остри респираторни инфекции. Приблизително 15 на сто. случаи, синдромът се появява след обилна диария, в 5 процента. - след хирургични манипулации, независимо дали става дума за аборти, херниотомия, апендектомия или по-сложни операции. Понякога заболяването се развива след различни видове ваксинации. GBS се среща във всяка част на света, по всяко време на годината, еднакво често и при двата пола. Средната възраст в повечето наблюдения е около 40 години. В същото време се разграничават два малки възрастови пика: на 20-25 години и над 60 години. В класическите случаи диагнозата GBS е проста и включва два задължителни признака: нарастваща мускулна слабост в поне два крайника и значително намаляване до пълна загуба на сухожилни рефлекси. Допълнителни диагностични критерии са намаляване на скоростта на провеждане на нервния импулс през мускулите с образуването на блок на проводимостта и протеиново-клетъчна дисоциация в цереброспиналната течност. Синдромът на Guillain-Barré се основава на автоимунни механизми, където ролята на провокиращ фактор се възлага на определени вируси и бактерии. Въпреки това, все още няма окончателно становище относно природата на антигена или антигените, които причиняват развитието на каскадни имунни реакции. През последните пет години е установено, че цял набор от полиневропатии се обединява под името GBS: остра възпалителна демиелинизираща полиневропатия (среща се в 75-80% от случаите); остра моторна невропатия и, като неин вариант, остра моторно-сензорна аксонална невропатия (15-20 процента); Синдром на Фишер (3%). Повечето автоимунни заболявания са необратими. Но при GBS картината е съвсем различна, уникална: болестта се самоограничава. Ако на тежко болен в продължение на няколко месеца се прави само изкуствена белодробна вентилация, засегнатите нерви се възстановяват. И почти толкова пълно, колкото при използването на основните съвременни методи за лечение на GBS - плазмафереза или интравенозна терапия с имуноглобулини от клас G. Може да възникне въпросът: защо да лекувате пациент със скъпи методи? Но представете си какво означава да си на вентилатор 3-6 месеца и да си прикован на легло? Навременното използване на плазмафереза и имуноглобулини от клас G може да намали времето, прекарано на механична вентилация до няколко седмици и дори дни, фундаментално да промени хода и изхода на заболяването. Не е тайна, че днес в страната много пациенти с тежки форми на GBS умират. Това до голяма степен се дължи на факта, че много болници не са оборудвани с висококачествена дихателна апаратура или нямат квалифициран персонал за продължителна изкуствена белодробна вентилация. Пациентите умират поради банални инфекции и рани от залежаване. В допълнение, далеч не навсякъде има възможност за извършване на операции по плазмафереза със замяна на големи обеми плазма (до 200 ml плазма / kg за курс на лечение, състоящ се от 4-5 операции). Абсолютно недопустимо е такива пациенти да се лекуват в селска или малка областна болница - те трябва да бъдат хоспитализирани в по-големи болници, оборудвани с необходимата материална база и оборудване. Типична грешка в много случаи е лечението на пациенти с GBS с хормонални препарати: специални изследвания на повече от хиляда пациенти показват, че хормоните не влияят на скоростта на възстановяване на нарушените функции, а напротив, носят много усложнения. Хормоните обаче продължават да се използват необосновано дори в редица клиники в най-големите руски градове. В чужбина за това те могат просто да бъдат лишени от медицински лиценз. Ако говорим за финансовата страна на въпроса, разбира се, днес за повечето пациенти лечението с вносни имуноглобулини от клас G, които се използват широко на Запад, просто не е достъпно, но, за щастие, курсът на програмна плазмафереза в нашата страна е много по-евтина. И терапевтичният ефект от тези два метода на лечение е един и същ: приблизително 85-90 процента. от случаите, човек със синдром на Гилен-Баре, въпреки най-тежкото увреждане на периферната нервна система, се възстановява напълно и само 10-15 процента. пациентите изпитват остатъчни ефекти. Разбира се, разпространението на синдрома на Guillain-Barré е несравнимо с инсулт, травматично увреждане на мозъка или епилепсия. Но при инсулт в най-добрия случай се възстановяват 20 процента. хора и навременното лечение на синдрома на Guillain-Barré с не по-малка тежест на лезията дава много по-голям ефект. И ако всяка година около 200 души страдат от SSS само в Москва, това е много за пълно възстановяване на здравето на 180 души. В моята практика имаше случай, когато болестта порази 18-годишен младеж, кандидат за майстор на спорта по лека атлетика: той не можеше да диша, да преглъща, да се движи сам. Година по-късно този човек изпълни стандарта на майстор на спорта. И има много такива примери - след правилно лечение на GBS младите жени раждат деца, по-голямата част от пациентите се връщат към пълноценен живот.
Синоними: остра демиелинизираща полирадикуло(невро)патия, остра постинфекциозна полиневропатия, синдром на Landry-Guillain-Barré, остаряла. Възходяща парализа на Ландри.
Срок Синдром на Guillain-Barréе епоним (т.е. дава име) за набор от синдроми на автоимунна остра възпалителна полирадикулоневропатия, характеризиращи се с прогресивна симетрична вяла парализа в мускулите на крайниците и мускулите, инервирани от черепните нерви (с възможно развитие на опасни респираторни и гълтателни нарушения) с или без чувствителни и вегетативни нарушения (нестабилно кръвно налягане, аритмии и др.).
Доста често заболяването се развива непосредствено след прехвърлените инфекции. В класическата версия на синдрома се наблюдава възходяща (от краката) тетрапареза (пареза (парализа) на четирите крайника).
Диагнозата се основава на анализ на характерната клинична картина и се потвърждава от изследване на цереброспиналната течност и електромиография (ЕМГ).
Лечението на синдрома на Guillain-Barré се извършва в интензивното отделение под контрола на функциите на дишане и преглъщане. Основните методи на специфична терапия са приблизително еднакво ефективна плазмафереза и интравенозна импулсна терапия с имуноглобулин G. Добро възстановяване на парализираните мускули се наблюдава в приблизително 75-85% от случаите.
Наред с факта, че синдромът на Guillain-Barré класически се представя като демиелинизираща полиневропатия с нарастваща слабост, наречена остра възпалителна демиелинизираща полиневропатия и представляваща 75-80% от случаите, няколко атипични варианта или подвида на този синдром са описани и идентифицирани в литература, представляваща хетерогенна група имунозависими периферни невропатии: синдром на Милър-Фишър (3 - 5%), остра моторна аксонална полиневропатия и остра сензомоторна аксонална полиневропатия (съставляват 15-20%) и по-рядко остра сензорна полиневропатия, остра пандиавтономия, остра краниална полиневропатия, фаринго-цервико-брахиален вариант. Като правило, тези варианти са клинично обикновено по-трудни от основния.
- Епидемиология
Синдромът на Guillain-Barré е най-честата остра полиневропатия. Заболеваемостта е 1,7 - 3,0 на 100 000 души от населението годишно, приблизително еднаква при мъжете и жените, няма сезонни колебания и се среща по-често в напреднала възраст. Заболеваемостта на възраст 15 години е 0,8 - 1,5, а на възраст 70 - 79 години достига 8,6 на 100 000. Смъртността е от 2 до 12%.
- Код по МКБ-10 G.61.0
Лечение
- Основни положения
- Лечението на синдрома на Guillain-Barré включва два компонента: неспецифична поддържаща терапия и специфична терапия с плазмафереза или пулсова терапия с имуноглобулин клас G.
- Поради възможността за развитие на декомпенсация с тежка дихателна недостатъчност в рамките на няколко часа, както и сърдечни аритмии, е необходимо лечение на синдрома на Guillain-Barré в острата фаза като спешност. В случай на развитие на остра дихателна недостатъчност в лечебно заведение трябва да е възможно провеждането на продължителна изкуствена вентилация на белите дробове.
- В тежки случаи с ранно развитие на остра дихателна недостатъчност, лечението се провежда в интензивно отделение или интензивно отделение. Провежда се ежечасно наблюдение на VC, кръвни газове, кръвни електролити, сърдечна честота, кръвно налягане, състояние на булбарните мускули (поява и увеличаване на нарушения на преглъщането, които не водят до облекчаване на кашлицата, дрезгав глас, нарушения на говора). При булбарна парализа с нарушения на преглъщането, задушаване, изливане на напитката през носа е показано въвеждането на назогастрална сонда и често интубация (за предотвратяване на аспирация и аспирационна пневмония). Трахеалната интубация с механична вентилация е показана с развитието на дихателна недостатъчност, ако VC падне под 12-15 ml / kg и с булбарна парализа и нарушено преглъщане и говор - под 15-18 ml / kg. При липса на тенденция за възстановяване на спонтанното дишане в рамките на 2 седмици се извършва трахеостомия.
- Кортикостероидите в момента не се използват, тъй като е доказано, че са неефективни. Те не подобряват изхода от заболяването.
- Специфична терапия
Специфична терапия с плазмафереза или интравенозно приложение на високи дози имуноглобулин започва скоро след диагностицирането. Показана е приблизително еднаква ефективност на двата метода на лечение, както и липсата на допълнителен ефект от комбинацията от тези методи. В момента няма консенсус относно избора на специфична терапия.
Като се има предвид, че има голяма вероятност за спонтанно възстановяване, лечението на пациенти с лек синдром на Guillain-Barré може да бъде ограничено до неспецифична и поддържаща терапия. При умерена тежест на процеса и особено при тежки случаи специфичната терапия започва възможно най-рано.
Лечението с имуноглобулин има известно предимство пред плазмаферезата, тъй като е по-лесно и по-удобно за използване, има значително по-малък брой странични ефекти, по-лесно е за пациента и следователно имуноглобулинът е лекарството на избор при лечението на синдрома на Guillain-Barré .
- Интравенозна импулсна терапия с имуноглобулинИнтравенозната пулсова терапия с имуноглобулин (IgG, лекарства - октагам, сандоглобулин, интраглобулин, нормален човешки имуноглобулин) е показана при пациенти, които не могат да извървят повече от 5 m без чужда помощ, или при по-тежки (с парализа, респираторни и гълтателни нарушения) пациенти с максимална ефективност на лекарството в началото на терапията в рамките на 2 до 4 седмици от началото на заболяването. Прилага се интравенозно в доза от 0,4 g / kg / ден в продължение на 5 дни (обща курсова доза от 2 g / kg или около 140 g). Алтернативна схема за прилагане на същата курсова доза: 1 g / kg / ден в две дози за два дни. Употребата му е ограничена от високата цена.
- ПлазмаферезаПлазмаферезата, приложена във фазата на прогресиране на заболяването (приблизително през първите две седмици), почти удвоява процеса на възстановяване и намалява остатъчния дефект. Предписва се в умерени и тежки случаи по схема от 4-6 сесии през ден, с обмен на 50 ml / kg на сесия (най-малко 35-40 ml плазма на kg телесно тегло), за общ. курс от 200-250 ml / kg (най-малко 160 ml плазма на 1 kg телесно тегло на курс). При леки случаи и във фазата на възстановяване плазмаферезата не е показана. Плазмаферезата показа доста висока ефективност, когато се прилага при тежко болни пациенти, когато терапията е започнала повече от 30 дни след началото на заболяването.
При 5-10% от пациентите се наблюдава рецидив на заболяването след края на лечението с плазмафереза или имуноглобулин. В този случай или възобновете лечението със същия метод, или използвайте алтернативен метод.
- Неспецифична терапия и рехабилитация
- Необходимо е да се предотврати дълбока венозна тромбоза на долния крак при лежащо болни (особено с парализа на краката). Антикоагуланти с непряко действие фенилин или варфарин се прилагат перорално в дози, стабилизиращи INR на ниво 2,0, или фраксипарин (надропарин) 0,3 ml. s / c 1 - 2 пъти / ден или сулодексид (Wessel Due F) 2 пъти на ден, 1 ампула (600 LSU) / m в продължение на 5 дни, след това перорално 1 капсула (250 LSU) 2 пъти на ден. Профилактиката се извършва преди времето, когато пациентът започне да става от леглото. Ако се е развила тромбоза преди началото на терапията, профилактиката се извършва по същата схема. Използва се и превръзка с еластична превръзка на краката до средата на бедрото (или се използват чорапи с градуирана компресия) и повдигане на краката с 10-15º. Показано е пасивно и, ако е възможно, активно "ходене в леглото" с огъване на краката, излъчващо ходене за 5 минути 3-5 пъти на ден.
- При пареза на лицевите мускули се предприемат мерки за защита на роговицата: вливане на капки за очи, превръзка през нощта
- Предотвратяване на контрактури и парализа. За да направите това, пасивните упражнения се извършват 1-2 пъти на ден, те осигуряват правилната позиция в леглото (удобно легло, опори за краката), масажират крайниците. След това се включват активни физиотерапевтични упражнения.
- Предотвратяване на рани от залежаване - сменяйте позицията в леглото на всеки 2 часа, избършете кожата със специални съединения, използвайте антидекубитални матраци.
- Предотвратяване на белодробна инфекция под формата на дихателни упражнения, възможно най-ранна мобилизация на пациента. При намаляване на жизнения капацитет на белите дробове, затруднено отделяне на бронхиалните секрети се показва масаж (усилие и вибрации при завъртане на тялото в легнало положение) на всеки 2 часа през деня.
- Симптоматична терапия: антиаритмично, хипотензивно, аналгетично. При артериална хипотония, спадане на кръвното налягане (приблизително кръвно налягане 100 - 110/60 - 70 mm Hg и по-ниско), интравенозно се прилагат колоидни или кристалоидни разтвори (изотоничен разтвор на натриев хлорид, албумин, полиглюкин) и в случай на недостатъчност ефект в комбинация с кортикостероиди: преднизолон 120 - 150 мг., дексазон 8 - 12 мг.. При недостатъчност на тези средства се използват вазопресори: допамин (50 - 200 мг. се разрежда в 250 мл. изотоничен разтвор на натриев хлорид и прилага се със скорост 6 12 капки / мин), или норепинефрин, или мезатон. При умерена болка се използват прости аналгетици и нестероидни противовъзпалителни средства. При силен болков синдром се използва трамал или кабамазепин (тигретол) или габапентин (невронтин), възможно в комбинация с трициклични антидепресанти (имипрамин, амитриптилин, азафен и др.).
- Занимания с логопед за лечение и профилактика на нарушения на речта и гълтането.
- Рехабилитацията включва масаж, лечебна гимнастика, физиотерапия. При мускулни болки и парези на крайниците се извършва транскутанна мускулна стимулация.
Цялото съдържание на iLive се преглежда от медицински експерти, за да се гарантира, че е възможно най-точно и фактическо.
Имаме строги указания за снабдяване и цитираме само реномирани уебсайтове, академични изследователски институти и, където е възможно, доказани медицински изследвания. Обърнете внимание, че числата в скоби (и т.н.) са връзки към такива проучвания, върху които може да се кликне.
Ако смятате, че някое от нашето съдържание е неточно, остаряло или по друг начин съмнително, моля, изберете го и натиснете Ctrl + Enter.
Синдромът на Guillain-Barré (остър идиопатичен полиневрит; парализа на Landry; остра възпалителна демиелинизираща полирадикулоневропатия) е остра, обикновено бързо прогресираща, възпалителна полиневропатия, характеризираща се с мускулна слабост и лека загуба на дистална чувствителност. Автоимунно заболяване. Диагноза по клинични данни. Лечение на синдрома на Guillain-Barré: плазмафереза, y-глобулин, по показания изкуствена вентилация на белите дробове. Резултатът от синдрома се подобрява значително с адекватно поддържащо лечение в интензивно отделение и използване на съвременни методи за имуномодулираща терапия.
, , , , , , ,
Код по МКБ-10
G61.0 Синдром на Гилен-Баре
Епидемиология
Заболеваемостта е от 0,4 до 4 случая на 100 000 души население годишно. Синдромът на Guillain-Barré се наблюдава във всички възрастови групи, но по-често при хора на възраст 30-50 години, с еднаква честота при мъжете и жените. Расовите, географските и сезонните различия в честотата на синдрома на Guillain-Barré обикновено не са характерни, с възможното изключение на острата моторна аксонална невропатия, която е най-често срещана в Китай и обикновено се свързва с чревна инфекция поради Campylobacter jejuniи следователно малко по-често се срещат през лятото.
Заболеваемостта нараства значително след 40-годишна възраст. Синдромът на Гилен-Баре убива средно 600 души годишно в Съединените щати. Следователно синдромът на Guillain-Barré е много важен здравен проблем, особено важен за възрастните хора.
, , , , ,
Причини за синдрома на Гилен-Баре
Най-честата придобита възпалителна невропатия. Автоимунният механизъм не е напълно разбран. Известни са няколко варианта: в някои преобладава демиелинизацията, в други страда аксонът.
В около 2/3 от случаите синдромът се появява 5 дни до 3 седмици след инфекциозно заболяване, операция или ваксинация. В 50% от случаите заболяването е свързано с инфекция Campylobacter jejuni,ентеровируси и херпесни вируси (включително цитомегаловирус и вируси, които причиняват мононуклеоза), както и Mycoplasma spp.През 1975 г. имаше огнище, свързано с програмата за ваксиниране срещу свински грип.
, , , , ,
Патогенеза
Демиелинизацията и възпалителната инфилтрация в корените на гръбначните нерви и проксималните нерви могат да обяснят клиничното представяне на синдрома на Guillain-Barré. Смята се, че в патогенезата на заболяването участват както хуморалният, така и клетъчният имунитет. Наличието на лимфоцити и макрофаги в перивенозните зони и тяхното взаимодействие с миелинизирани аксони показват преди всичко възможната роля на автоимунните реакции в процеса на демиелинизация. Тази позиция се потвърждава от по-ранни наблюдения, според които имунизацията на лабораторни животни с адювантен периферен миелин причинява експериментален алергичен неврит. Въпреки че по-късно беше показано, че пречистените миелинови протеини - например миелинов основен протеин P2 или P2 пептидни фрагменти и PO протеинът - могат да причинят експериментална невропатия, антитела срещу тези съединения рядко се откриват при синдрома на Guillain-Barré. Т клетки, изолирани от далака и лимфните възли на плъхове, имунизирани с Р2-синтетичен пептид 53-78, могат експериментално да възпроизведат тежък експериментален алергичен неврит при сингенни мишки. По този начин клетъчните и, вероятно, хуморалните имунни механизми могат да медиират създаването на експериментален модел на възпалително увреждане на периферните нерви.
Последните проучвания насочиха вниманието към ролята на глюкоконюгатите и липополизахаридите на миелиновата обвивка, клетъчната мембрана на Schwann или аксоналната мембрана като основни антигени, иницииращи възпалителния/имунния отговор при синдрома на Guillain-Barré. При подробно изследване, проведено в Япония, са идентифицирани антигени при пациенти Campylobacter jejuni. В това изследване методът Penner е използван за откриване на термостабилни липополизахариди, а методът на Lior е използван за откриване на термолабилни протеинови антигени. PEN 19 и LIO 7 антигени C. jejuniса по-често изолирани при пациенти със синдром на Guillain-Barré (съответно в 52 и 45% от случаите), отколкото при пациенти със спорадичен ентерит, причинен от C. jejuni(съответно 5 и 3%) и са свързани с повишаване на титъра на антителата срещу GM1 (вероятно поради наличието на GMl-подобен липополизахариден антиген). Според съобщения от други страни инфекцията C. jejuniмного по-малко вероятно е да предшестват развитието на GBS. В допълнение, процентът на пациентите с антиганглиозидни антитела е много по-променлив, вариращ от 5% до 60%. Освен това не е открита връзка между наличието на антитела срещу GM1 и клиничните и електрофизиологични прояви на заболяването.
При синдрома на Miller Fisher често се откриват антитела срещу GQlb. Използвайки имунохистохимични методи, GQlb беше открит в паранодалната област на човешките черепни нерви, инервиращи очите. Установено е, че анти-GQlb антителата могат да блокират предаването в нервно-мускулната система на мишки.
При аксоналния двигателен вариант на синдрома на Guillain-Barré, заболяването е по-често предшествано от инфекция с C. jejuni и антитела срещу GM1 ганглиозид и продукт за активиране на комплемента C3d се свързват с аксолемата на моторните влакна.
Анти-GMI антителата могат също да се свържат с възлите на Ranvier, като по този начин нарушават провеждането на импулси. В допълнение, тези антитела са способни да причинят дегенерация на окончанията на моторните влакна и интрамускулните аксони, което наскоро беше показано при пациенти с остра моторна аксонална полиневропатия. Ентеритът, причинен от C. jejuni, може да провокира синдром на Guillain-Barré чрез увеличаване на производството на гама-делта Т-лимфоцити, които могат активно да участват във възпалителни/имунни процеси. Високите серумни нива на тумор некротизиращ фактор-алфа (TNF-a), но не и интерлевкин-1b или разтворим рецептор на интерлевкин-2, корелират с електрофизиологичните промени при синдрома на Guillain-Barré. Изследването на проби от аутопсията показва, че поне в някои случаи на класическата остра възпалителна демиелинизираща форма на синдрома на Guillain-Barré е включен комплемент - това се показва от откриването на C3d и C5d-9 компоненти на външната повърхност на Schwann клетки, които образуват мембранен атакуващ комплекс.
По този начин повечето от компонентите, които обикновено участват в патогенезата на имуномедиираните заболявания, присъстват в синдрома на Guillain-Barré. Въпреки че има вероятност антителата срещу глюкоконюгати да участват в патогенезата на няколко различни клинични форми на синдрома на Guillain-Barré, точната им роля е неизвестна. Дори ако има антитела срещу GM1, те могат да се свържат не само с GM1, но и с други гликолипиди или гликопротеини, които имат подобни въглехидратни места. В тази връзка специфичните антигени на Schwann клетките или аксоналната мембрана, срещу които е насочена възпалителната/имунна реакция, както и възможната роля на имуноглобулините, изискват изясняване. Освен това, в много случаи на синдром на Guillain-Barré, няма данни за предходна или съпътстваща инфекция. C. jejuni,антитела срещу GM1 или черти на друг микроорганизъм, чиито антигени могат да инициират имунен отговор (например чрез молекулярна мимикрия).
Изследването на материали, получени от нервна биопсия и аутопсия, показва, че клетъчните имунни механизми също допринасят за развитието на синдрома на Guillain-Barré. При тежки случаи на синдром на Guillain-Barré, лимфоцитите и макрофагите присъстват в двигателните влакна от корените до окончанията, а активираните макрофаги са в близък контакт с миелина или фагоцитират миелина. Въпреки че са получени данни в експериментален модел на възпалителна невропатия, които потвърждават участието на Т-лимфоцитите в увреждането на нервите, няма убедителни доказателства, че това се случва при пациенти със синдром на Guillain-Barré. Натрупаните до момента данни подкрепят участието на активирани Т-лимфоцити, които преминават кръвно-мозъчната бариера и инициират демиелинизация заедно с антитела срещу специфични антигени на нервните влакна, цитокини (като TNF-a и интерферон-y), компоненти на комплемента, вероятно включително мембранно атакуващ комплекс и активирани макрофаги. Необходими са повече изследвания, за да се изясни ролята на всеки от тези елементи, както и последователността, в която те участват в патогенезата на синдрома на Guillain-Barré.
, , , , , , , , , , ,
Симптоми на синдрома на Гилен-Баре
Симптомите на синдрома на Guillain-Barré са преобладаването на отпусната пареза (колкото по-проксимално, толкова по-дълбоко), нарушенията на чувствителността са по-слабо изразени. Обикновено почти симетричната слабост с парестезии започва в краката, по-рядко в ръцете или главата. В 90% от случаите слабостта достига максимум на 3-та седмица от заболяването. Загуба на дълбоки сухожилни рефлекси. Функцията на сфинктерите е запазена. При тежки случаи слабостта на лицевите и орофарингеалните мускули е очевидна в половината от случаите. В 5-10% от случаите се налага интубация и механична вентилация поради парализа на дихателната мускулатура.
Понякога (очевидно с вариантна форма) се развива изразена автономна дисфункция с колебания в кръвното налягане, анормална секреция на антидиуретичен хормон, аритмии, чревна стаза, задържане на урина и нарушена реакция на зеницата към светлина. Синдромът на Fisher е рядък вариант на синдрома на Guillain-Barré и включва офталмоплегия, атаксия и арефлексия.
Първите симптоми, редът на тяхното появяване и динамиката
Обикновено синдромът на Guillain-Barré започва с мускулна слабост и/или сензорни нарушения (изтръпване, парестезия) в долните крайници, които се разпространяват към горните крайници след няколко часа или дни.
Първите симптоми на Guillain-Barré са сензорни нарушения, като парестезии в краката. Въпреки че обективните признаци на сензорно увреждане са чести, те обикновено са леки. Ранните и изключително неприятни прояви на заболяването за пациентите могат да бъдат дълбоки болки в гърба и болезнени дизестезии в крайниците. Парализата може първоначално да обхване долните крайници и след това бързо да се разпространи нагоре в продължение на няколко часа или дни до горните крайници, мимичните, булбарните и дихателните мускули. Възможно е обаче и друго развитие на събитията, когато заболяването започва със слабост на мимическите мускули и горните крайници, след което засяга долните крайници. От самото начало симптомите обикновено са симетрични, а парализата е придружена от загуба или отслабване на сухожилните и периосталните рефлекси. Вегетативните влакна често участват в синдрома на Guillain-Barré. Автономните симптоми се откриват в около 50% от случаите, но функцията на сфинктера обикновено не се засяга. Заболяването има монофазен ход: период на нарастване на симптомите, продължаващ няколко дни или седмици, е последван от период на плато, продължаващ от няколко дни до няколко месеца, след което възстановяването настъпва за няколко месеца. През 1976-1977 г. има леко увеличение на случаите на синдром на Guillain-Barré, свързан с имунизация с ваксина срещу свински грип, но не е регистриран подобен феномен при имунизация с друга версия на ваксината срещу грип през 1980-1988 г.
В класическите случаи, проявяващи се чрез комбинация от моторни, сензорни и автономни симптоми, които се основават на демиелинизираща полирадикулоневропатия, диагнозата на синдрома на Guillain-Barré рядко е трудна. Съществува обаче и аксонален вариант на синдрома на Guillain-Barré, проявяващ се предимно с двигателни нарушения и остра моторно-сензорна аксонална невропатия. Острата аксонална форма обикновено се проявява с по-тежък функционален дефект и има по-лоша прогноза. Комбинацията от офталмоплегия, атаксия и арефлексия е характерна за друг вариант на синдрома на Guillain-Barré, известен като синдром на Miller Fisher. От диагностична гледна точка, при липса на симптоми на увреждане на черепните нерви, дори при непокътната функция на сфинктера, е необходимо да се изключи компресията на гръбначния мозък с помощта на невроизобразяване. При диференциалната диагноза е важно да се има предвид и остра интермитентна порфирия, метална интоксикация, която може да причини остра полиневропатия, както и системни заболявания като инфекциозна мононуклеоза, паранепластични синдроми или различни метаболитни нарушения. ХИВ-инфектираните пациенти са предразположени към развитие на полиневропатия или полирадикулоневропатия, които могат да бъдат свързани със синдром на Guillain-Barré, цитомегаловирусна полирадикулоневропатия или лимфом. Тези състояния са трудни за диференциране въз основа само на клиничното представяне, но изследването на цереброспиналната течност при ХИВ-асоциирана полирадикулоневропатия обикновено разкрива неутрофилна плеоцитоза и данни за вирусна репликация.
Вегетативната дисфункция (включително нарушения на настаняването, коремна и гръдна болка, артериална хипотония, тахикардия) може значително да влоши състоянието на пациента и да служи като неблагоприятен прогностичен признак. В едно проучване, субклинични признаци на засягане както на симпатиковата, така и на парасимпатиковата нервна система, открити чрез тестове за автономни функции, са отбелязани при по-голямата част от пациентите.
Скала за тежест на двигателния дефицит в Северна Америка
- Една трета от пациентите развиват дихателна недостатъчност.
- В повечето случаи има нарушения на повърхностната чувствителност под формата на лека или умерена хипо- или хиперестезия от полиневритичен тип (като "чорапи и ръкавици"). Често се отбелязва болка в бедрата, лумбалната и глутеалната област. Те могат да бъдат ноцицептивни (мускулни) или невропатични (поради увреждане на сетивните нерви). При приблизително половината от пациентите се откриват дълбоки нарушения на чувствителността (особено вибрации и мускулно-ставно усещане), които са много груби (до пълна загуба).
- При повечето пациенти се наблюдават лезии на черепните нерви. В процеса е възможно да се включат всякакви черепни нерви (с изключение на I и II двойки), но поражението на VII, IX и X двойки се наблюдава с най-голямо постоянство, което се проявява чрез пареза на лицевите мускули и булбарни нарушения .
- Вегетативните нарушения се наблюдават при повече от половината пациенти и могат да бъдат представени от следните нарушения.
- Преходна или персистираща артериална хипертония или по-рядко артериална хипотония.
- Сърдечни аритмии, най-често синусова тахикардия.
- Нарушение на изпотяването [локална (ръце, крака, лице) или обща хиперхидроза].
- Стомашно-чревни нарушения (запек, диария, в редки случаи чревна непроходимост).
- Дисфункцията на тазовите органи (обикновено задържане на урина) е рядка и обикновено лека и преходна.
- При синдрома на Милър-Фишър клиничната картина е доминирана от атаксия, която обикновено има характеристики на малкия мозък, в редки случаи - смесен (мозъчно-чувствителен), и частична или пълна офталмоплегия, могат да бъдат засегнати и други черепни нерви (VII, IX , Х). Парезата обикновено е лека, в една четвърт от случаите има нарушения на чувствителността.
, , , ,
Диагностични критерии за синдрома на Guillain-Barré
, , , , , , ,
Признаци на синдрома на Гилен-Баре, необходими за диагностициране
- А. Прогресивна мускулна слабост в повече от един крайник
- B. Арефлексия (липса на сухожилни рефлекси)
Характеристики на синдрома на Гилен-Баре в подкрепа на диагнозата
- A. Клинични характеристики (изброени по важност)
- Прогресия: Мускулната слабост се развива бързо, но спира да прогресира в рамките на 4 седмици от началото.
- Относителна симетрия: симетрията рядко е абсолютна, но ако единият крайник е засегнат, противоположният също е засегнат (коментар: пациентите често съобщават за асиметрични симптоми в началото на заболяването, но до момента на физикалния преглед лезиите обикновено са симетрични).
- Субективни и обективни симптоми на сензорни нарушения.
- Увреждане на черепните нерви: пареза на лицевите мускули.
- Възстановяване: обикновено започва 2-4 седмици след като заболяването спре да прогресира, но понякога може да се забави с няколко месеца. Повечето пациенти получават пълно възстановяване на функцията.
- Вегетативни нарушения: тахикардия и други аритмии, постурална артериална хипотония, артериална хипертония, вазомоторни нарушения.
- Липса на треска в началото на заболяването (в някои случаи е възможна треска в началото на заболяването поради интеркурентни заболявания или други причини; наличието на треска не изключва синдрома на Guillain-Barré, но увеличава вероятността от друго заболяване , по-специално полиомиелит).
- Б. Опции
- Тежки сензорни нарушения с болка.
- Прогресия за 4 седмици. Понякога е възможно прогресиране на заболяването в продължение на много седмици или наличие на малки рецидиви.
- Прекратяване на прогресията без последващо възстановяване или персистиране на тежки персистиращи остатъчни симптоми.
- Функции на сфинктерите: обикновено сфинктерите не се засягат, но в някои случаи са възможни нарушения на уринирането.
- Засягане на ЦНС: Синдромът на Guillain-Barré засяга периферната нервна система и няма надеждни доказателства за възможността за засягане на ЦНС. Някои пациенти имат груба церебеларна атаксия, необичайни признаци на крака от екстензорен тип, дизартрия или неясно ниво на сензорно увреждане (което предполага проводен тип увреждане), но те не изключват диагнозата синдром на Guillain-Barré, ако са налице други типични симптоми .
- C. Промени в ликвора, подкрепящи диагнозата
- Протеин: 1 седмица след началото на заболяването концентрацията на протеин в цереброспиналната течност се повишава (през първата седмица може да е нормално).
- Цитоза: съдържанието на мононуклеарни левкоцити в цереброспиналната течност е до 10 в 1 µl (при съдържание на левкоцити 20 в 1 µl или повече е необходимо задълбочено изследване. Ако съдържанието им е над 50 в 1 µl, диагнозата синдром на Guillain-Barré се отхвърля; изключение правят пациенти с HIV инфекция и лаймска борелиоза).
Признаци на синдрома на Guillain-Barré, които пораждат съмнения относно диагнозата
- Изразена персистираща асиметрия на парезата.
- Устойчиви тазови нарушения.
- Наличието на тазови нарушения в началото на заболяването.
- Съдържанието на мононуклеарни левкоцити в цереброспиналната течност е повече от 50 в 1 µl.
- Наличието на полиморфонуклеарни левкоцити в цереброспиналната течност.
- Ясно ниво на сензорни нарушения
Признаци на синдрома на Гилен-Баре, които изключват диагнозата
- Текуща злоупотреба с летливи органични разтворители (злоупотреба с вещества).
- Нарушения на порфириновия метаболизъм, предполагащи диагноза остра интермитентна порфирия (повишена уринна екскреция на порфобилиноген или аминолевулинова киселина).
- Скорошна дифтерия.
- Наличие на симптоми на невропатия, дължащи се на интоксикация с олово (пареза на мускулите на горния крайник, понякога асиметрична, с тежка слабост на екстензора на ръката) или данни за интоксикация с олово.
- Наличието на изключително сензорни увреждания.
- Надеждна диагноза на друго заболяване, проявяващо се със симптоми, подобни на синдрома на Guillain-Barré (полиомиелит, ботулизъм, токсична полиневропатия).
Форми
В момента в рамките на синдрома на Guillain-Barré има четири основни клинични варианта.
- Острата възпалителна демиелинизираща полирадикулоневропатия е най-честата (85-90%) класическа форма на синдрома на Guillain-Barré.
- Аксоналните форми на синдрома на Guillain-Barré се наблюдават много по-рядко (10-15%). Острата моторна аксонална невропатия се характеризира с изолирана лезия на моторни влакна, най-често срещана в Азия (Китай) и Южна Америка. При остра моторно-сензорна аксонална невропатия са засегнати както моторните, така и сетивните влакна, тази форма е свързана с продължителен курс и лоша прогноза.
- Синдромът на Miller-Fisher (не повече от 3% от случаите) се характеризира с офталмоплегия, церебеларна атаксия и арефлексия с обикновено лека пареза.
В допълнение към основните, напоследък се разграничават още няколко нетипични форми на заболяването - остра пандизавтономия, остра сензорна невропатия и остра черепна полиневропатия, които се наблюдават много рядко.
, , , , , , ,
Диагностика на синдрома на Гилен-Баре
При събиране на анамнеза трябва да се изяснят следните аспекти.
- Наличие на провокиращи фактори. В приблизително 80% от случаите развитието на синдрома на Guillain-Barré се предшества от определени заболявания или състояния в рамките на 1-3 седмици.
- - Инфекции на стомашно-чревния тракт, горните дихателни пътища или друга локализация. Асоциация с чревна инфекция, причинена от Campylobacter jejuni.Преживелите кампилобактериоза са приблизително 100 пъти по-склонни да развият синдром на Guillain-Barré в рамките на 2 месеца от заболяването, отколкото общата популация. Синдромът на Guillain-Barré може да се развие и след инфекции, причинени от херпесни вируси (цитомегаловирус, вирус на Epstein-Barr, варицела-зостер), Haemophilus influenzae,микоплазми, морбили, паротит, лаймска борелиоза и др. В допълнение, синдромът на Guillain-Barré може да се развие с HIV инфекция.
- Ваксинация (против бяс, против тетанус, срещу грип и др.).
- Хирургични интервенции или наранявания от всякаква локализация.
- Приемане на определени лекарства (тромболитични лекарства, изотретиноин и др.) или контакт с токсични вещества.
- Понякога синдромът на Guillain-Barré се развива на фона на автоимунни (системен лупус еритематозус) и туморни (лимфогрануломатоза и други лимфоми) заболявания.
Лабораторни и инструментални изследвания
- Общи клинични изследвания (обща кръвна картина, общ анализ на урината).
- Биохимичен кръвен тест: серумна електролитна концентрация, газов състав на артериалната кръв. При планиране на специфична терапия с имуноглобулини от клас G е необходимо да се определят Ig фракциите в кръвта. Ниската концентрация на IgA обикновено се свързва с неговия наследствен дефицит, в такива случаи рискът от развитие на анафилактичен шок е висок (имуноглобулиновата терапия е противопоказана).
- Изследвания на CSF (цитоза, концентрация на протеин).
- Серологични изследвания при съмнение за етиологична роля на определени инфекции (маркери на HIV, цитомегаловирус, вирус на Epstein-Barr, Borrelia burgdorferi, Campylobacter jejuniи т.н.). Ако се подозира полиомиелит, са необходими вирусологични и серологични (титър на антитела в двойки серуми) изследвания.
- ЕМГ, резултатите от които са от основно значение за потвърждаване на диагнозата и определяне на формата на синдрома на Guillain-Barré. Трябва да се има предвид, че резултатите от ЕМГ може да са нормални през първата седмица от заболяването.
- Методите за невроизображение (MRI) не позволяват потвърждаване на диагнозата синдром на Guillain-Barré, но може да са необходими за диференциална диагноза с патология на ЦНС (остър мозъчно-съдов инцидент, енцефалит, миелит).
- Мониторинг на функцията на външното дишане [определяне на жизнения капацитет на белите дробове (VC) за навременно идентифициране на индикации за прехвърляне на пациента към механична вентилация.
- В тежки случаи (особено при бърза прогресия на заболяването, булбарни нарушения, тежки автономни нарушения), както и по време на механична вентилация, е необходимо да се наблюдават основните жизнени показатели (в интензивното отделение): кръвно налягане, ЕКГ, пулс оксиметрия, дихателна функция и други (в зависимост от конкретната клинична ситуация и терапия).
, , ,
Неврофизиологични критерии за класификация на синдрома на Guillain-Barré
Нормално (всички от следните признаци трябва да присъстват във всички изследвани нерви)
- Дистална моторна латентност
- Устойчивост и латентност на F-вълната
- CRV >100% долна граница на нормата.
- Амплитудата на М-отговора по време на стимулация в дисталната точка е >100% от долната граница на нормата.
- Амплитудата на М-отговора по време на стимулация в проксималната точка е >100% от долната граница на нормата.
- Съотношението „Амплитуда на М-отговора по време на стимулация в проксималната точка / амплитуда на М-отговора по време на стимулация в дисталната точка“> 0,5
Първична демиелинизираща лезия (изисква поне един от признаците в поне два изследвани нерва или наличие на два признака в един нерв, ако всички останали нерви не са възбудими и амплитудата на М-отговора при стимулация в дисталната точка е > 10% от долната граница на нормата).
- Дистална моторна латентност >110% горна граница на нормата (>120%, ако амплитудата на М-отговора по време на стимулация в дисталната точка
- Съотношението „Амплитуда на М-отговор по време на стимулация в проксималната точка / амплитуда на М-отговор по време на стимулация в дистална точка“ е 20% от долната граница на нормата.
- Латентност на F-вълната >120% горна граница на нормата
Първична аксонална лезия
- Липсата на всички горепосочени признаци на демиелинизация във всички изследвани нерви (наличието на един от тях в един от нервите е приемливо, ако амплитудата на М-отговора по време на стимулация в дисталната точка
Раздразнителност на нервите
- М-отговорът не може да бъде предизвикан в нито един от нервите при стимулация в дисталната точка (или е възможно да се предизвика само в един нерв с неговата амплитуда
Несигурно поражение
Не отговаря на критериите за нито една от горните форми
Тази форма може да включва случаи на първична тежка аксонопатия, тежка дистална демиелинизация с блок на проводимостта и вторична Wallerian дегенерация след демиелинизация; неврофизиологично е невъзможно да се направи разлика между тях.
Показания за консултация с други специалисти
- Лечението на пациенти с тежки форми на синдрома на Guillain-Barré се извършва съвместно с лекаря на отделението за интензивно лечение.
- При тежки сърдечно-съдови нарушения (упорита тежка артериална хипертония, аритмии) може да се наложи консултация с кардиолог.
Данни от допълнителни методи на изследване
Електромиографията (ЕМГ) има голяма диагностична стойност при синдрома на Guillain-Barré. и изследване на скоростта на импулсите по нервите, както и изследване на цереброспиналната течност. Започвайки от 3-7-ия ден след появата на първите симптоми, електрофизиологичното изследване разкрива забавяне на проводимостта по двигателните и (в по-малка степен) по сетивните влакна, удължаване на дисталната латентност и латентния период на F-вълната, намаляване на амплитудата на общия потенциал на мускулно действие (М-отговор) и понякога сензорни потенциали на действие, както и фокални и асиметрични блокове на проводимост, които са показателни за сегментна демиелинизираща полиневропатия. От друга страна, при остра моторна аксонална полиневропатия, амплитудата на сензорните потенциали на действие и скоростта на провеждане по сетивните влакна може да са нормални, но има намаление на амплитудата на общия мускулен потенциал на действие и само леко забавяне на проводимостта по двигателните влакна. Когато са засегнати както двигателните, така и сетивните влакна, както общият потенциал на мускулно действие, така и потенциалът на сетивното действие могат да бъдат грубо променени, а дисталната латентност и скоростта на провеждане могат да бъдат трудни за измерване, което предполага тежка моторна сензорна аксонопатия. При синдрома на Miller Fisher, проявяващ се с атаксия, офталмоплегия и арефлексия, мускулната сила остава непокътната, а ЕМГ и скоростта на нервната проводимост може да са нормални.
При изследване гръбначно-мозъчна течностпри пациенти със синдром на Guillain-Barré се открива повишаване на съдържанието на протеин до ниво над 60 mg / dl при нормална цитоза (не повече от 5 клетки в 1 μl). Въпреки това, в първите дни на заболяването съдържанието на протеин в цереброспиналната течност може да бъде нормално, докато увеличаването на цитозата до 30 клетки на 1 μl не изключва диагнозата синдром на Guillain-Barré.
Тъй като биопсията на суралния нерв обикновено не разкрива признаци на възпаление или демиелинизация, този метод не е включен в стандартния набор от изследвания при повечето пациенти със синдром на Guillain-Barré, но може да бъде важен в научните изследвания. Патологичните изследвания показват, че при синдрома на Guillain-Barré са засегнати предимно проксималните нерви и корените на гръбначните нерви: именно в тях се откриват оток, сегментна демиелинизация и инфилтрация на ендоневриума от мононуклеарни клетки, включително макрофаги. Мононуклеарните клетки взаимодействат както с Schwann клетките, така и с миелиновата обвивка. Въпреки че синдромът на Guillain-Barré е полирадикулоневропатия, патологични промени могат да бъдат открити и в централната нервна система (ЦНС). В повечето от 13-те случая на аутопсия е открита мононуклеарна инфилтрация с лимфоцити и активирани макрофаги в гръбначния мозък, продълговатия мозък и моста. Първичната демиелинизация обаче не е открита в ЦНС. В дългосрочен курс преобладаващият тип възпалителни клетки в централната и периферната нервна система са активирани макрофаги, освен това там се откриват CD4 + и CD8 + Т-лимфоцити.
, , , , , , , , , , , ,
Диференциална диагноза
Синдромът на Guillain-Barré трябва да се диференцира от други заболявания, проявяващи се с остра периферна пареза, предимно от полиомиелит (особено при малки деца) и други полиневропатии (дифтерия, с порфирия). В допълнение, лезиите на гръбначния мозък и мозъчния ствол (напречен миелит, инсулт във вертебробазиларната система) и заболявания с нарушена нервно-мускулна трансмисия (миастения гравис, ботулизъм) могат да имат подобна клинична картина.
- При диференциална диагноза с полиомиелит трябва да се вземат предвид данните от епидемиологичната история, наличието на треска в началото на заболяването, симптоми от страна на стомашно-чревния тракт, асиметрия на лезията, липса на обективни нарушения на чувствителността и висока цитоза в цереброспиналната течност. Диагнозата полиомиелит се потвърждава чрез вирусологично или серологично изследване.
- Полиневропатията при остра интермитентна порфирия може да прилича на синдрома на Guillain-Barré, но като правило е придружена от различни психопатологични симптоми (налудности, халюцинации и др.) И силна коремна болка. Диагнозата се потвърждава чрез откриване на повишена концентрация на порфобилиноген в урината.
- Трансверзалният миелит се характеризира с ранна и персистираща дисфункция на тазовите органи, наличие на ниво на сензорни нарушения и липса на увреждане на черепните нерви.
- Симптоми, наподобяващи тези при синдрома на Guillain-Barré, са възможни при обширни инфаркти на мозъчния ствол с развитие на тетрапареза, която в острия период има периферни характеристики. Въпреки това, такива случаи се характеризират с остро развитие (обикновено в рамките на няколко минути) и в повечето случаи потискане на съзнанието (кома), което не се наблюдава при синдрома на Guillain-Barré. Окончателната диагноза се потвърждава от ЯМР.
- Миастения гравис се различава от синдрома на Guillain-Barré по променливостта на симптомите, липсата на сензорни нарушения и характерни промени в сухожилните рефлекси. Диагнозата се потвърждава чрез ЕМГ (откриване на феномен на намаляване) и фармакологични тестове.
- Ботулизмът, в допълнение към съответните епидемиологични данни, се характеризира с низходящ тип разпространение на пареза, запазване на сухожилните рефлекси в някои случаи, липса на сензорни нарушения и промени в цереброспиналната течност.
Лечение на синдрома на Guillain-Barré
Целите на лечението на синдрома на Гилен-Баре са поддържане на жизнените функции, облекчаване на автоимунния процес с помощта на специфична терапия и предотвратяване на усложнения.
Показания за хоспитализация
Всички пациенти със синдром на Guillain-Barré подлежат на хоспитализация в болница с интензивно отделение и интензивно отделение.
Нелекарствено лечение на синдрома на Guillain-Barré
Приблизително 30% от случаите на синдром на Guillain-Barré развиват тежка дихателна недостатъчност (поради пареза на диафрагмата и дихателните мускули), което налага механична вентилация. Показания за интубация с по-нататъшна механична вентилация - намаляване на VC до 15-20 ml / kg, P и O 2 50 mm Hg. Продължителността на механичната вентилация (от няколко дни до месеци) се определя индивидуално, като се фокусира върху жизнения капацитет, възстановяването на рефлекса на преглъщане и кашлица и общата динамика на заболяването. Изключете пациента от вентилатора постепенно, през етапа на интермитентна принудителна вентилация.
При тежки случаи с тежка пареза правилното лечение е от основно значение за предотвратяване на усложнения, свързани с продължителна неподвижност на пациента (рани от налягане, инфекции, тромбоемболични усложнения и др.): периодична (на всеки 2 часа или повече) промяна на позицията на пациент, грижа за кожата, профилактика аспирация [санация на устата и носа, хранене през назогастрална сонда, санация на трахеята и бронхите (при механична вентилация)], контрол на функциите на пикочния мехур и червата, пасивна гимнастика и масаж на крайниците, и т.н.
При персистираща брадиаритмия със заплаха от асистолия може да се наложи инсталиране на временен пейсмейкър.
Медикаментозно лечение и плазмафереза
Като специфична терапия за синдрома на Guillain-Barré, насочена към спиране на автоимунния процес, в момента се използва пулсова терапия с имуноглобулини от клас G и плазмафереза. Методите за специфична терапия са показани за тежък (според северноамериканската скала за тежест на двигателния дефицит 4 и 5 точки) и умерен (2-3 точки) ход на заболяването. Ефективността на двата метода е приблизително еднаква, едновременното им прилагане е непрактично. Методът на лечение се избира индивидуално, като се вземат предвид наличността, възможните противопоказания и др.
- Плазмаферезата е ефективно лечение на синдрома на Guillain-Barré, значително намалява тежестта на парезата, продължителността на механичната вентилация и подобрява функционалния резултат. Обикновено се извършват 4-6 операции с интервал от един ден; обемът на плазмата, която трябва да бъде заменена при една операция, трябва да бъде най-малко 40 ml/kg. Като заместителна среда се използват 0,9% разтвор на натриев хлорид, реополиглюкин и разтвор на албумин. Плазмаферезата е относително противопоказана при чернодробна недостатъчност, тежка патология на сърдечно-съдовата система, нарушения на кръвосъсирването и наличие на инфекции. Възможни усложнения са хемодинамични нарушения (спад на кръвното налягане), алергични реакции, електролитни нарушения, хеморагични нарушения, развитие на хемолиза. Всички те са доста редки.
- Имуноглобулин клас G се прилага интравенозно в доза 0,4 g/kg веднъж дневно в продължение на 5 дни. Лечението с имуноглобулин, подобно на плазмаферезата, намалява продължителността на престоя на апаратна вентилация и подобрява функционалния резултат. Най-честите нежелани реакции са главоболие и мускулни болки, треска, гадене; тяхната тежест може да бъде намалена чрез намаляване на скоростта на инфузия. Изключително редки са тежки нежелани реакции, като тромбоемболия, асептичен менингит, хемолиза, остра бъбречна недостатъчност и др. Нормалният човешки имуноглобулин е противопоказан при вроден дефицит на IgA и анамнеза за анафилактични реакции към имуноглобулинови препарати.
Симптоматично лечение на синдрома на Guillain-Barré
- Инфузионна терапия за корекция на нарушения на киселинно-базовия, водно-електролитния баланс, тежка артериална хипотония.
- При персистираща тежка артериална хипертония се предписват антихипертензивни лекарства (бета-блокери или блокери на бавни калциеви канали).
- При тежка тахикардия се предписват бета-блокери (пропранолол), при брадикардия - атропин.
- При развитието на интеркурентни инфекции е необходима антибиотична терапия (използват се широкоспектърни лекарства, като флуорохинолони).
- За профилактика на дълбока венозна тромбоза и белодробна емболия се предписва нискомолекулен хепарин в профилактични дози два пъти дневно).
- При болка от ноцицептивен произход (мускулна, механична) се препоръчва парацетамол или НСПВС, при невропатична болка лекарствата на избор са габапентин, карбамазепин, прегабалин.
Хирургично лечение на синдрома на Guillain-Barré
Ако е необходима продължителна (повече от 7-10 дни) механична вентилация, препоръчително е да се приложи трахеостомия. При тежки и продължителни булбарни нарушения може да се наложи гастростомия.
Общи принципи за лечение на синдрома на Гилен-Баре
Лечението на остро развиващите се и бързо нарастващи прояви на синдрома на Guillain-Barré изисква поддържащо лечение в интензивното отделение, както и излагане на имунните механизми на заболяването. Пациентите със синдром на Guillain-Barré трябва да бъдат хоспитализирани за внимателно проследяване на дихателните и автономните функции. Колкото по-бързо се натрупва парализата, толкова по-вероятно е да се наложи механична вентилация. В периода на нарастване на симптомите са необходими редовни неврологични прегледи, оценка на белодробния капацитет, поддържане на проходимостта на дихателните пътища с редовно изсмукване на слуз. В ранен стадий на заболяването е необходима постоянна бдителност, тъй като дори при липса на очевидни нарушения на дихателните и булбарните функции, малката аспирация може значително да увеличи автономната дисфункция и да провокира дихателна недостатъчност.
Подобрението в прогнозата и намаляването на смъртността при синдрома на Guillain-Barré, постигнато през последните години, се дължи главно на ранното приемане на пациенти в интензивни отделения. Показания за прехвърляне на пациента в отделението за интензивно лечение и разглеждане на въпроса за интубация може да бъде намаляване на белодробния капацитет под 20 ml / kg и затруднено отстраняване на секретите от дихателните пътища. Целта на ранното прехвърляне е да се избегне спешна интубация в условията на тежка дихателна недостатъчност с драматични колебания в кръвното налягане и сърдечната честота, които могат да причинят дисфункция или миокарден инфаркт. Една от най-важните задачи на поддържащата терапия е предотвратяването и навременното лечение на белодробни и пикочни инфекции, както и предотвратяването на дълбока венозна тромбоза на крака и последваща белодробна емболия чрез подкожно приложение на хепарин (5000 IU 2 пъти на ден) . Също така е необходимо да се следи храненето и работата на червата. Тъй като автономната дисфункция има значително влияние върху смъртността, е необходимо постоянно проследяване на сърдечната дейност и кръвното налягане.
Един от важните аспекти на подпомагането на пациенти със синдром на Guillain-Barré в интензивното отделение, който обаче не винаги се взема предвид, е коригирането на тежка тревожност, която може да бъде причинена от пълно обездвижване на пациента на фона на на непокътната интелигентност. В това отношение е важна психологическата подкрепа. Пациентите трябва да обяснят същността на заболяването, характеристиките на неговия ход, включително възможността за прогресия, да се запознаят с методите на лечение на различни етапи. Важно е да им се обясни, че вероятността за пълно възстановяване е много висока, дори ако са на апаратна вентилация известно време. Установяването на контакт с помощта на движенията на очите намалява чувството на пациента за изолация от света. Според нашия опит, прилагането на 0,5 mg лоразепам на всеки 4-6 часа е ефективно при нощни халюцинации. Също така е възможно да се предпише 0,5 mg рисперидон или 0,25 mg оланзапин.
Практиката за лечение на синдрома на Guillain-Barré претърпя значителни промени през последното десетилетие. Например, доказана е ефективността на плазмаферезата. Въпреки че механизмът му на действие остава неизвестен, се смята, че той може да бъде свързан с екскрецията на антитела, цитокини, комплемент и други медиатори на имунния възпалителен отговор. Отворено, многоцентрово проучване в Северна Америка, сравняващо резултатите между плазмафереза и липса на специфично лечение, показа, че пет последователни дни плазмафереза намалява болничния престой и води до по-голямо подобрение в сравнение с контролите. Лечението е по-ефективно, ако започне през първата седмица на заболяването. Подобни резултати са получени от French Cooperative Group, която провежда рандомизирано многоцентрово проучване и показва, че четири сесии на плазмафереза водят до по-бързо възстановяване при 220 пациенти, включени в проучването (French Cooperative Group, 1987). Проучване на същите пациенти година по-късно показа, че пълното възстановяване на мускулната сила е отбелязано при 71% от пациентите, подложени на плазмафереза, и само при 52% от пациентите в контролната група (French Cooperative Group, 1992). Следващото проучване сравнява ефективността на различни сесии на плазмафереза при 556 пациенти със синдром на Guillain-Barré с различна тежест на симптомите (French Cooperative Group, 1997). При пациенти с леки симптоми, които са претърпели две сесии на плазмафереза, възстановяването е по-значимо, отколкото при пациенти, чийто режим на лечение не включва плазмафереза. При умерено симптоматични пациенти четири сесии на плазмафереза са по-ефективни от две сесии на плазмафереза. В същото време шест сесии на плазмафереза не надвишават четири сесии по отношение на ефективността при пациенти с умерени и тежки симптоми. В момента повечето центрове, специализирани в лечението на синдрома на Guillain-Barré, все още използват пет до шест сесии, които се провеждат в продължение на 8-10 дни, за да се избегне стресът, свързан с ежедневната процедура. Обменното кръвопреливане се извършва с помощта на катетър Shealy. Плазмаферезата е ефективна и при деца със синдром на Guillain-Barré, като ускорява процеса на възстановяване на способността за самостоятелно движение. Въпреки че плазмаферезата е сравнително безопасна процедура, използването й при синдрома на Guillain-Barré изисква специално внимание поради опасността от автономна дисфункция при пациентите и тяхната склонност към развитие на инфекции.
Интравенозното приложение на високи дози имуноглобулин също е признато за ефективно лечение на синдрома на Guillain-Barré, което може значително да намали продължителността и тежестта на заболяването. Както в случая с плазмаферезата, механизмът на терапевтичното действие на имуноглобулина остава неясен. Предполага се, че може да елиминира патогенни антитела, дължащи се на антиидиотипни антитела, да блокира Fc компонента на антителата върху целевите клетки, а също така да инхибира отлагането на комплемента, да разтваря имунните комплекси, да отслабва функциите на лимфоцитите, да нарушава производството или да пречи на прилагането на цитокини функции. Имуноглобулинът се предписва в обща доза от 2 g / kg, която се прилага в продължение на 2-5 дни. В рандомизирано проучване, сравняващо ефекта на имуноглобулина и плазмаферезата, беше показано, че при плазмаферезата подобрението настъпва средно след 41 дни, а при имуноглобулина - след 27 дни. В допълнение, пациентите, които са получили имуноглобулин, са имали значително по-малко усложнения и са имали нужда от механична вентилация в по-малка степен. Старостта е основният неблагоприятен прогностичен фактор. Последващо рандомизирано многоцентрово проучване на плазмафереза и имуноглобулин при 383 пациенти, на които са предписани тези методи през първите 2 седмици след появата на симптомите, показва, че и двата метода имат сравнима ефикасност, но комбинацията им няма значителни предимства пред използването на всеки от методите поотделно. .
Въвеждането на имуноглобулин в доза от 2 g/kg за 2 дни се оказа ефективен и безопасен метод за лечение на деца с тежък синдром на Guillain-Barré. Страничните ефекти са леки и се наблюдават рядко. Някои пациенти, особено страдащите от мигрена, са имали главоболие, което понякога е придружено от асептичен менингит с плеоцитоза в цереброспиналната течност. Понякога се наблюдават и втрисане, треска и миалгия, както и остра бъбречна дисфункция с развитие на бъбречна недостатъчност. При въвеждането на имуноглобулин е възможна анафилактична реакция, особено при лица с дефицит на имуноглобулин А. Основният недостатък както на имуноглобулина, така и на плазмаферезата е високата цена. Въпреки това, това очевидно е по-малко от ефективността на тези лечения, което е очевидно дори в тази ера на правене на пари.
В двойно-сляпо, плацебо-контролирано, многоцентрово проучване при 242 пациенти със синдром на Guillain-Barré, високите дози интравенозни кортикостероиди (метилпреднизолон, 500 mg дневно в продължение на 5 дни) не повлияват никоя от мерките за изход за синдрома на Guillain-Barré. Barre, както и вероятността от повторната му поява. В последващо отворено проучване, при което 25 пациенти със синдром на Guillain-Barré са лекувани с IV имуноглобулин (0,4 g/kg/ден за 5 дни) и метилпреднизолон (500 mg/ден за 5 дни), ефектът е сравнен с получените контролни данни по-рано с използването на един имуноглобулин. При комбинация от имуноглобулин и метилпреднизолон възстановяването е по-добро, докато 76% от пациентите до края на 4-та седмица показват подобрение на поне едно функционално ниво - в контролната група подобна степен на възстановяване е отбелязана само при 53% на пациентите. Това може да предполага, че кортикостероидите все още могат да играят роля в лечението на синдрома на Guillain-Barré. Необходими са рандомизирани клинични проучвания, за да се изясни този въпрос и да се определи дали има значително подобрение в резултата от заболяването, когато интравенозните кортикостероиди се добавят към плазмафереза или имуноглобулин.
По-нататъшно управление
След края на острия период са необходими комплексни рехабилитационни мерки, чийто план се изготвя индивидуално, в зависимост от тежестта на остатъчните симптоми (ЛФК, масаж и др., докато топлинните процедури са противопоказани!).
Пациентите, които са имали синдром на Guillain-Barré, трябва да бъдат информирани за необходимостта от спазване на защитен режим най-малко 6-12 месеца след края на заболяването. Физическо претоварване, прегряване, хипотермия, прекомерна инсолация, прием на алкохол са неприемливи. Също така през този период трябва да се въздържате от ваксинация.
Прогноза
Смъртността при синдрома на Гилен-Баре е средно 5%. Причината за смъртта може да бъде дихателна недостатъчност, смърт е възможна и поради аспирационна пневмония, сепсис и други инфекции, белодробна емболия. Смъртността нараства значително с възрастта: при деца под 15 години тя не надвишава 0,7%, докато при хората над 65 години достига 8,6%. Други неблагоприятни прогностични фактори за пълно възстановяване включват дълъг (повече от 1 месец) период на механична вентилация, наличие на предишни белодробни заболявания.
Повечето пациенти (85%) получават пълно функционално възстановяване в рамките на 6-12 месеца. Постоянните остатъчни симптоми персистират в приблизително 7-15% от случаите. Предиктори за неблагоприятен функционален резултат са възраст над 60 години, бързо прогресиращо протичане на заболяването и ниска амплитуда на М-отговора при стимулация в дисталната точка (което предполага тежко увреждане на аксоните). Честотата на рецидивите на синдрома на Guillain-Barré е приблизително 3-5%.
